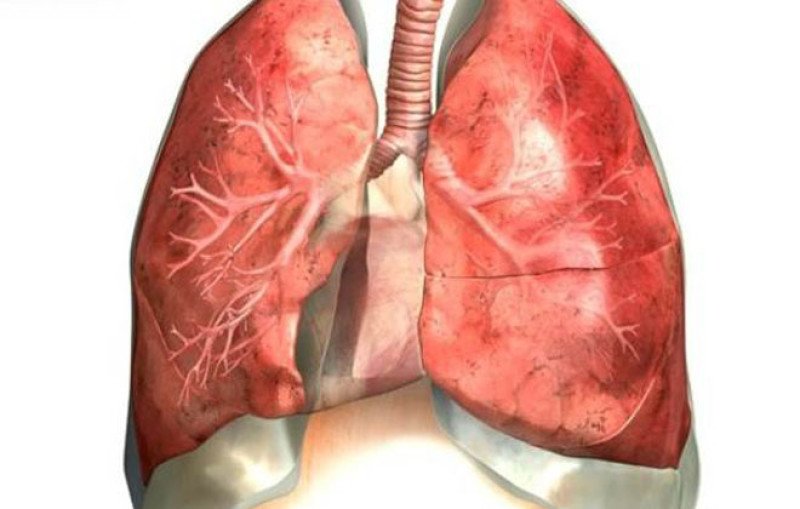
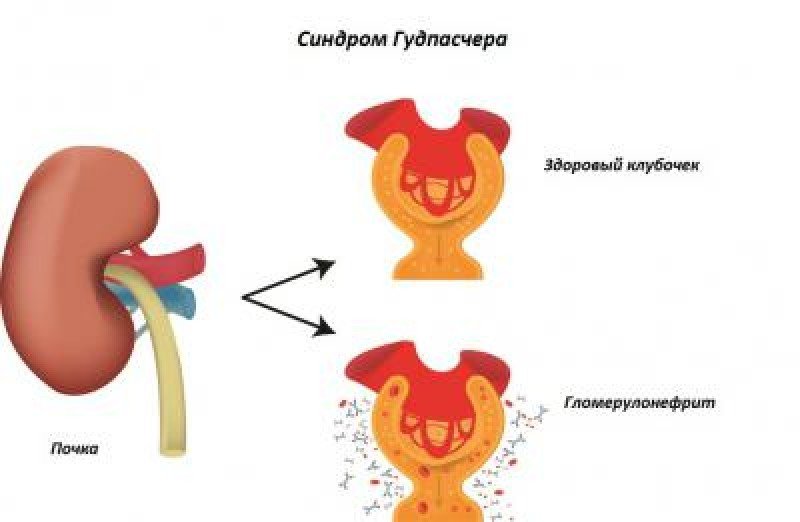
Синдром Гудпасчера
Синдром Гудпасчера – имунновоспалительное заболевание мелких сосудов почек и легких. Это заболевание может возникнуть абсолютно в любом возрасте, но чаше всего синдром встречается у молодых мужчин. Синдром Гудпасчера у детей, подростков и пожилых людей встречается редко и обнаруживается после дифференциального диагноза.
Внимание!
Здесь вы сможете выбрать врача, занимающегося лечением Синдром Гудпасчера Если вы не уверены в диагнозе, запишитесь на прием к терапевту или врачу общей практики для уточнения диагноза.
Статьи на тему Синдром Гудпасчера:
Причины
Симптомы
Диагностика
Лечение
Формы синдрома Гудпасчера
По скорости развития симптомов выделяют две формы заболевания:
- бурное прогрессирование:
- преобладает почечная и легочная симптоматика;
- летальный исход наступает спустя 11–12 месяцев в результате легочного кровотечения или почечной недостаточности.
- периоды прогрессирования чередуются с периодами полного отсутствия симптомов;
- если лечение началось своевременно, продолжительность жизни может составить от 2 до 12 лет.
Причины
Причины синдрома Гудпасчера:
- причина возникновения синдрома неизвестна, но выявлена непосредственная связь с бактериальной и вирусной инфекциями, а также приемом некоторых препаратов: иммуносупрессивных, противовоспалительных, цитостатиков;
- синдром Гудпасчера может развиться под воздействием химических и физических факторов внешней среды (органические растворители, действие углеводородов, пар лаков, бензина), на фоне онкозаболеваний;
- при систематическом употреблении кокаина также описаны случаи развития данного заболевания; ;
- аутоиммунная причина развития заболевания является наиболее распространенной, при ней происходит выработка антител к определенным структурам легких и почек.
Симптомы
Симптомы синдрома Гудпасчера проявляются в следующем:
- основной признак заболевания – это сочетание симптомов гломерулонефрита с кровохарканьем (признак распада легочной ткани);
- появляются периферические отеки (отеки лица, живота, ног);
- отмечается малокровие (анемия);
- прогрессирующая боль в грудной клетке, кашель, одышка;
- выраженное недомогание, слабость, похудение;
- периодически наблюдается повышение температуры тела;
- воспаление глаз;
- уменьшение объема мочи;
- появление крови в моче;
- артериальное давление повышается от 140/90 мм рт. ст. и выше.
Диагностика
- анализ анамнеза заболевания и жалоб – какие симптомы появились и когда, обращался ли пациент к врачу, как изменялись симптомы со временем, какие обследования и лечения проводились и каковы их результаты;
- анализ анамнеза жизни, при котором уточняются данные о наличии вредных привычек, о хронических заболеваний и о перенесенных ранее заболеваниях;
- анализ семейного анамнеза, при котором уточняется, встречалось ли подобное заболевание у родственников (например, быстропрогрессирующий гломерулонефрит);
- общий анализ крови – позволит обнаружить любые признаки воспалительного процесса в организме (значительное повышение уровня скорости оседания эритроцитов, повышение уровня лейкоцитов, высокое содержание ретикулоцитов);
- биохимический анализ крови – позволит обнаружить повышенный уровень остаточного азота и понижение содержания сывороточного железа;
- анализ мочи, который позволит обнаружить следующие изменения:
- протеинурию, при которой в моче обнаруживается белок;
- гематурию, при которой в моче обнаруживается кровь;
- цилиндрурию;
- как правило, в осадке моче обнаруживают эритроциты, лейкоциты, эритроцитарные и зернистые цилиндры.
Лечение
В лечение синдрома Гудпасчера входит следующее:
- раннее назначение крупных доз иммуносупрессантов и кортикостероидов;
- плазмаферез – с целью немедленного удаления антител, циркулирующих в крови (это процедура, в ходе которой у пациента берется порция крови, из которой удаляется плазма, а затем кровяные клетки возвращают обратно в сосуды);
- гемодиализ, с помощью которого проходит очищение и фильтрация крови вне организма;
- симптоматическая терапия, которая включает назначение препарата железа и повторные переливания крови.
Осложнения
Если у пациента выявлен синдром Гудпасчера, на сегодняшний день все доступные методы лечения не могут обеспечить полного излечения или предотвращения обострения:
Синдром гудпасчера
Синдром Гудпасчера – является заболеванием аутоиммунного вида, при протекании его страдают мелкие сосуды в почках и легких по той причине, что организм непроизвольно начинает выработку к ним аутоантител.
Причины
Выявить главную первопричину данных патологических процессов не удалось до сих пор. Однако исследования не прекращаются, ученые смогли установить тонкую взаимосвязь с появлением воспалительного процесса вирусного/бактериального происхождения.
Также создать благоприятную почву для синдрома могут сильные антивоспалительные, иммуносупрессивные препараты, снижающие работу иммунной системы и приостанавливающие деление клеток.
- зависимость от кокаина;
- регулярный контакт с вредными химическими веществами (парами бензина, углеводорода, резкими запахами, органическими растворителями); ;
- онкологические заболевания; / СПИД;

Абсцесс лёгкого
В зависимости от проявления симптоматики и характера течения болезни различают три формы:
- быстрое развитие симптомов – характеризуется иммуновоспалительными патологиями, поражающими клубочки почек (гломерулонефрит) и почечной недостаточностью;
- медленное течение – периоды времени с проявлением признаков чередуются с полным отсутствием какой-либо симптоматики, при правильном лечении длительность жизни пациента может составлять от нескольких до 12 лет;
- постоянно прогрессирующая геморрагическая пневмония и гломерулонефрит – чаще всего летальный исход наступает в течение года, это считается злокачественным типом заболевания.
Симптомы
Признаки, по которым можно судить о наличии подобного патологического процесса в организме:
-
;
- сильный кашель, со временем прогрессирующий;
- периферическая отечность ног, лица и живота;
- наличие кровяных элементов при мочеиспускании (гематурия);
- двустороннее почечное воспаление иммунного типа; ; , головокружения, потеря сознания;
- воспалительный процесс в слизистой оболочке глаз;
- быстрая потеря веса;
- бледность кожных покровов;
- слабость, вялость;
- общее плохое самочувствие;
- мышечная боль (миалгия);
- повышение температуры тела;
- малый объем мочи (олигурия);
- повышенное артериальное давление;
- болезненность в области грудной клетки;
- синюшная окраска кожи и слизистых оболочек (цианоз).
Возможными сопутствующими заболеваниями могут быть: острая почечная недостаточность, отек легких, легочное кровотечение, сердечная астма, артралгия, перикардит.

Сосуды почки в норме и при синдроме Гудпасчера
Диагностика
Для того чтобы выявить болезнь и начать лечение, следует записаться на прием к врачу-нефрологу или пульмонологу в зависимости от преобладающих проявлений. Помимо этого, понадобится консультация врача-ревматолога. На нашем сайте вы можете найти лучших частных врачей Москвы, прочитать отзывы об их практике и ознакомиться с ценовой политикой.
При прослушивании легких отчетливо проявляются сухие и влажные хрипы, врач проводит сбор информации о развитии синдрома и фиксирует клинические признаки.
Для подтверждения диагноза используются следующие диагностические приемы:
- общий анализ крови и мочи;
- проба по Зимницкому;
- биохимические пробы крови;
- лабораторное исследование мокроты;
- рентгенография легких;
- биопсия пораженных органов;
- электрокардиограмма;
- эхокардиография;
- спирометрия;
- ультразвуковая диагностика почек.
Лечение
Оздоровление в острой стадии синдрома Гудпасчера начинается с пульс-терапии с применением метилпреднизолона, иногда в сочетании с циклофосфаном. После того как критическая симптоматика будет снята, больного переводят на поддерживающую терапию.
Высокой эффективностью обладает плазмаферез. Во время этой процедуры проводится удаление части находящихся в крови антител. Это происходит путем отделения лимфы из некоторой порции крови и возвращения клеток обратно в кровеносную систему.
В случае появления признаков почечной недостаточности используется гемодиализ. Иногда требуется полное удаление почки и ее замена на трансплантант.
Для облегчения симптомов необходимы переливание эритроцитарной массы и кровяной плазмы, назначение медикаментов, содержащих железо.
Прогноз не является благоприятным, так как доступные в наше время методики не обеспечивают полного выздоровления. Однако при своевременном и качественном лечении существенно возрастает длительность жизни. Часто причиной летального исхода становится легочное кровотечение или ОПН.
Профилактика
За всю историю развития медицины выявлено только несколько случаев полного выздоровления. Однако соблюдение некоторых правил в состоянии значительно снизить риск развития недуга:
Синдром Гудпасчера
Синдром Гудпасчера представляет собой иммуно-воспалительное заболевание мелких сосудов легких и почек.
Симптомы Синдрома Гудпасчера:
Классической триадой, выражающей клинико-патогенетическую сущность этой болезни, являются легочные кровотечения, гломерулонефрит и антитела к антигенам основной мембраны капилляров легких и почек. Заболевание встречается редко и может поражать любой возраст, но чаще болеют молодые мужчины. Конкретные причины неизвестны; не раз описывалось развитие синдрома Гудпасчера после недавно перенесенного гриппа или вдыхания углеводородов. В связи с этим не исключено, что подобные воздействия таким образом изменяют химическую структуру упомянутых выше антигенов основных мембран, что они приобретают аутоантигенные свойства и вызывают продукцию соответствующих антител с патогенными свойствами.
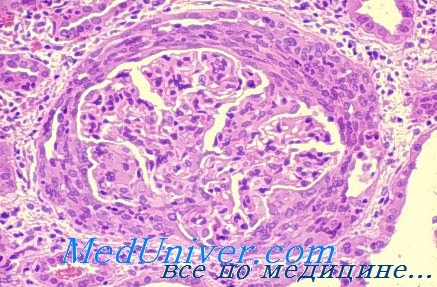
В тканях почек с помощью иммунофлюоресцентного метода обнаруживают линейные отложения антител к базальным мембранам, сочетающиеся в ряде случаев с отложениями фракции комплемента С3. В то же время при электронномикроскопическом исследовании не обнаруживают отложений иммунных комплексов. Циркулирующие антитела к базальным мембранам канальцев, клубочков и легочных альвеол в сыворотке крови обнаруживают более чем у 90% больных (особенно в ранней стадии заболевания), однако они не отражают тяжести органных изменений или общего прогноза, имея, таким образом, в основном диагностическое значение. Уровень сывороточного комплемента и циркулирующих иммунных комплексов в норме. При гистологическом исследовании почечные клубочки у некоторых больных могут выглядеть нормальными, но в большинстве случаев наблюдается явная патология – от очаговых пролиферативных изменений до некротического гломерулонефрита. Наиболее часто развиваются экстракапиллярные “полулуния”. В легких находят кровоизлияния в полость альвеол с картиной альвеолита или без нее.
В начале заболевания клинические проявления связаны прежде всего с поражением легких – кашель, небольшая одышка и особенно кровохарканье; реже наблюдается легкий цианоз. При аускультации возможны влажные хрипы. Рентгенологически характерны инфильтраты разной величины в обоих легких, особенно в прикорневых областях. В мокроте, как правило, обнаруживают макрофаги, содержащие железо. Повышенное отложение железа в легочной ткани может быть установлено сканированием с ^Ре. У многих больных имеют место лихорадка, боль в суставах, резкая общая слабость, но в ряде случаев эти симптомы выражены слабо или отсутствуют. У большинства больных с первых дней или недель заболевания регистрируют признаки гломерулонефрита. В анализах крови обнаруживают повышенную СОЭ и лейкоцитоз; позже в результате легочных кровотечений возможна гипохромная анемия.
Течение болезни в целом неблагоприятное, хотя и неоднотипное. На первых этапах основной угрозой являются легочные геморрагии, причем нередко больной умирает в результате первого и единственного профузного кровотечения. У ряда переживших это кровотечение может развиться относительная ремиссия легочного процесса, но во многих случаях кровохарканье и легочные геморрагии рецидивируют. Поражение почек у отдельных больных остается относительно нетяжелым, но в большинстве случаев быстро прогрессирует с развитием олигурической почечной недостаточности, приводящей к смерти в течение нескольких месяцев и даже недель. Средняя продолжительность жизни у неадекватно леченных больных составляет менее полугода.
Диагностика Синдрома Гудпасчера:
При дифференциальном диагнозе синдрома Гудпасчера следует иметь в виду, что сочетание легочного кровотечения с выраженной почечной патологией (в том числе с недостаточностью почек) может встретиться при гранулематозе Вегенера, узелковом полиартериите, СКВ, геморрагическом васкулите, криоглобулинемии, эмболии ветвей легочной артерии вследствие тромбоза почечной вены, болезни легионеров и даже при тяжелой недостаточности кровообращения с выраженным застоем в легких и почках. Однако все эти заболевания отличаются от синдрома Гудпасчера по клиническим признакам и отсутствию антител к антигенам базальных мембран.
Лечение Синдрома Гудпасчера:
Современная лекарственная терапия несколько улучшила прогноз синдрома Гудпасчера. При угрожающих легочных кровотечениях показано парентеральное введение метилпреднизолона по типу пульс-терапии (500-1000 мг в день), после чего переходят на длительный прием кортикостероидов внутрь (по 40- 80 мг преднизолона в сутки с очень медленным и постепенным снижением дозы). При отсутствии тяжелых кровотечений стероиды назначают внутрь с начала лечения. Имеются указания на нарастание эффекта в случаях их сочетания с длительным приемом иммунодепрессантов – азатиоприна или циклофосфамида по 150-200 мг в день. Значительное улучшение почечных изменений и практическая ремиссия легочного процесса описаны у больных, которым назначали повторные курсы плазмафереза (с обменом 2-4 л плазмы в день процедуры) в комбинации с рассмотренным выше лекарственным лечением. Положительный эффект наблюдался даже у больных с уже сформированными пролиферативными изменениями (“полулуниями”) в почечных клубочках. Следует помнить, что при легочных кровотечениях противопоказаны антикоагулянты, которые назначают при других васкулитах. У больных с почечной недостаточностью на фоне необратимых морфологических изменений (выраженный фиброз, облитерация клубочков, атрофия канальцев) рассчитывать на улучшение можно только в результате применения регулярного гемодиализа либо трансплантации почки (хотя в трансплантированной почке в последующем не исключается развитие гломерулонефрита). Обобщая, следует признать, что современная терапия привела к некоторому улучшению течения синдрома Гудпасчера, но не привела к принципиальным успехам. Тем не менее можно полагать, что заболевание в принципе обратимо, в пользу чего свидетельствуют единичные его спонтанные ремиссии.
К каким докторам следует обращаться если у Вас Синдром Гудпасчера:
Вас что-то беспокоит? Вы хотите узнать более детальную информацию о Синдрома Гудпасчера, ее причинах, симптомах, методах лечения и профилактики, ходе течения болезни и соблюдении диеты после нее? Или же Вам необходим осмотр? Вы можете записаться на прием к доктору .
Синдром Гудпасчера: симптомы, диагностика и лечение
Болезнь Гудпасчера характеризуется легочными кровотечениями и гломерулонефритом. Заболевание связано с выработкой антител, часто направленных против отдельных эпитопов коллагена IV типа в базальной мембране легочных альвеол и почечных клубочков. Причина неизвестна. Болезнь Гудпасчера следует отличать от синдрома Гудпасчера, при котором легочное кровотечение и гломерулонефрит обусловлены различными системными нарушениями, включая СКВ, геморрагический васкулит, узелковый полиартериит и гранулематоз Вегенера. У некоторых больных нефрит с антителами к базальной мембране почечных клубочков развивается в отсутствие легочного кровотечения и представляет собой одну из форм быстропрогрессирующего гломерулонефрита.
Патоморфология болезни Гудпасчера. Изменения при световой микроскопии в большинстве случаев напоминают быстропрогрессирующий гломерулонефрит. Иммунофлюоресцентная микроскопия выявляет линейные отложения IgG по ходу базальной мембраны клубочков.
Клинические проявления болезни Гудпасчера. Болезнь Гудпасчера редко встречается в детском возрасте. Обычно возникает кровохарканье, обусловленное легочным кровотечением, которое может быть опасным для жизни. Поражение почек проявляется острым нефритическим синдромом с гематурией, протеинурией и повышением АД и прогрессирует за несколько дней или недель. Уровень компонента комплемента С3 в сыворотке крови остается нормальным.
Диагностика болезни Гудпасчера. Биопсия почек позволяет предположить болезнь Гудпасчера. Присутствие в сыворотке антител к базальной мембране почечных клубочков подтверждает диагноз и исключает другие заболевания, сопровождающиеся синдромом Гудпасчера.
Прогноз и лечение болезни Гудпасчера. У больных, выживших после легочного кровотечения, обычно развивается терминальная стадия ХПН. Пульс-терапия метилпреднизолоном в сочетании с циклофосфамида и плазмаферезом увеличивает выживаемость и способствует устранению почечной патологии.

Гистология почек при болезни Гудпасчера
Гемолитико-уремический синдром
Гемолитико-уремический синдром (ГУС) — самая частая причина острой почечной недостаточности у маленьких детей, характеризуется микроангиопатической гемолитической анемией, тромбоцитопенией и уремией. Этот синдром сходен с тромботической тромбоцитопенической пурпурой, однако последняя обычно наблюдается у молодых женщин, рецидивирует, сопровождаясь лихорадкой, тяжелыми нарушениями ЦНС и тромбоцитопенией.
В развивающихся странах гемолитико-уремический синдром (ГУС) в 80 % случаев предшествует острый энтерит с поносом, вызываемый штаммом Escherichia coli (серотип 0157:Н1), который продуцирует веротоксин, близкий к цитотоксину Shigella dysenteriae. Этот микроб содержится в ЖКТ домашнего скота и попадает в организм человека с недожаренным мясом и непастеризованным молоком. Наблюдались вспышки заболевания после потреблении загрязненных напитков или купания в загрязненной воде.
Патоморфология гемолитико-уремического синдрома. Начальные изменения клубочков сводятся к утолщению стенок капилляров, сужению их просвета и разрастанию мезангия. При электронной микроскопии видно, что эти изменения обусловлены гранулярным отложением аморфного вещества неизвестного происхождения в субэндотелиальном слое и между капиллярами. В самих капиллярах и артериолах обнаруживаются фибриновые тромбы, которые могут приводить к некрозу коркового вещества почек.
В одних клубочках изменения прогрессируют вплоть до частичного или полного склероза, другие атрофируются вследствие ишемии. В пораженных мелких артериях и артериолах происходит концентрическая пролиферация интимы, закупоривая сосуды.
Патогенез гемолитико-уремического синдрома. Основную роль в патогенезе синдрома играет повреждение эндотелиальных клеток. Повреждение эндотелия почечных капилляров и артериол приводит к образованию отдельных тромбов. Диссеминированная внутрисосудистая коагуляция отмечается редко. Механическое повреждение эритроцитов при их прохождении через суженные участки сосуда обусловливает микроангиопатическую анемию. В основе тромбоцитопении лежат внутрипочечная адгезия или повреждение кровяных пластинок. Печень и селезенка удаляют поврежденные эритроциты и тромбоциты из кровотока. Эпизоды ГУС без диареи и отдельные семейные случаи могут объясняться отсутствием в плазме фактора, стимулирующего продукцию эндотелием простациклина, который расширяет сосуды и препятствует образованию тромбов.
Снижение уровня тромбомодулина, тканевого активатора плазминогена (алтеплазы) и гепариноподобных молекул, активирующих антитромбин III, напротив, способствует образованию тромбов при этом синдроме. Кроме того, еще до развития почечной патологии в сыворотке возрастает содержание таких прокоагулянтов, как фактор активации тромбоцитов, фрагменты протромбина 1 и 2, антиген тканевого активатора плазминогена, комплекс тканевого активатора и ингибитора плазминогена (ТАП-1), фактор Виллебранда, D-димеры и тромбоксан А2, которые и могут быть причиной тромбообразования.
Особенности течения и лечения синдрома Гудпасчера
Аутоиммунные патологии – распространенная на сегодняшний день проблема, которая, несмотря на это, изучена недостаточно. Во многих случаях причины и механизм развития недугов неизвестны, поэтому лечение сводится к симптоматической терапии. Одной из проблем, проявляющихся в результате нарушения работы защитных сил организма, является синдром Гудпасчера. Это заболевание, которое сопровождается синтезом антител против собственной базальной мембраны в альвеолах легких и клубочковом аппарате почек. Данная проблема опасна значительными воспалительными реакциями, которые приводят к формированию дыхательной и почечной недостаточности.
Впервые синдром Гудпасчера у детей и взрослых был описан в начале двадцатого века. В его течении отмечались гломерулонефрит и геморрагическое воспаление ткани легких. При этом на сегодняшний день болезнь относится к системным васкулитам – поражениям сосудов. Описанная в 1919 году американцем Э. У. Гудпасчером проблема была названа в его честь и подробно описана Петром Францевичем Литвицким в учебнике патофизиологии. Недуг относится к редким расстройствам. Чаще он регистрируется у пациентов в возрасте 20–30 и 50–60 лет, однако может быть выявлен и у ребенка. При подтверждении диагноза, связанного с аутоиммунным нарушением требуется проведение соответствующего лечения, при отсутствии которого крайне высока летальность.
Причины формирования синдрома Гудпасчера
Точный патогенез недуга на сегодняшний день неизвестен. Он связан с неадекватной реакцией организма на базальные мембраны собственных сосудов. Иммунитет отвечает выработкой антител против данных структур, что сопровождается сильной воспалительной реакцией. Именно она и приводит к развитию симптомов синдрома Гудпасчера. К основным причинам, способным спровоцировать формирование расстройства, относят:
- Ученые склоняются к участию в развитии недуга инфекционных и вирусных поражений. Возбудители подобных заболеваний приводят к формированию иммунного ответа, который в дальнейшем выходит из-под контроля, провоцируя возникновение васкулита.
- Значительное переохлаждение способно стать триггером в развитии синдрома. Это также связано с аномальной активностью защитных сил организма в ответ на стрессовое воздействие.
- К числу этиологических факторов заболевания относится и употребление лекарственных средств, обладающих влиянием на иммунитет. Это гормональные вещества, а также соединения, имеющие противовоспалительный эффект.
- Зарегистрированы данные и о генетической предрасположенности к формированию синдрома Гудпасчера. Они подтверждаются и наличием семейных случаев недуга.

Классификация и признаки патологии
Клиническую картину заболевания принято разделять на три вида:
- Самым опасным является злокачественный вариант развития проблемы. Он отличается быстрым прогрессированием и плохим прогнозом. Это связано со стремительным формированием гломерулонефрита, приводящего к почечной недостаточности. Проблема осложняется и признаками рецидивирующей пневмонии, которая носит геморрагический характер.
- При умеренном типе недуга симптомы развиваются не столь быстро. Как правило, клинические проявления имеют среднюю интенсивность, что дает время на диагностику заболевания.
- Медленный синдром Гудпасчера отличается развитием гломерулонефрита и прогрессированием почечной недостаточности. При этом респираторные признаки заболевания длительное время отсутствуют и проявляются уже на поздних стадиях расстройства.
Начало недуга, как правило, острое. Болезнь начинается с повышения температуры и одышки, кроме случаев медленного прогрессирования. Пациенты ощущают слабость, значительно теряют в весе. При развитии респираторных поражений возникает кровохарканье, которое сопровождается формированием анемии, что только усугубляет клиническую картину. Одновременно с симптомами расстройства функций легких прогрессирует гломерулонефрит. Он приводит к уменьшению суточного объема мочи, развитию артериальной гипертензии и интоксикации организма. Почечная недостаточность при синдроме Гудпасчера может сформироваться всего за несколько дней.
Диагностика
Подтверждение проблемы начинают со сбора анамнеза и осмотра. Кожа и слизистые оболочки пациентов бледные, на конечностях и лице присутствуют отеки. При аускультации выявляются влажные хрипы в легких. Диагностика синдрома Гудпасчера требует также проведения анализов крови и мочи, в которых находят изменения, характерные для анемии, воспалительных поражений и нарушения функции почек. Важным в подтверждении недуга является и рентген, который позволяет сделать фото легких. На снимках присутствуют множественные патологические очаги. Это связано с формированием своеобразных полостей, а также с изменением структуры сосудистого рисунка. Рентгенограмма при синдроме Гудпасчера хотя и не имеет ключевого значения, помогает дифференцировать проблему от ряда других, сопровождающихся сходными симптомами.
Обследование при данном аутоиммунном расстройстве обязательно включает специфический тест на определение антител к базальной мембране клубочкового аппарата почек. Используются и морфологические анализы, для которых требуется забор материала при помощи биопсии. В качестве дополнительных методов применяют УЗИ, ЭхоКГ и ЭКГ.
Лечение и прогноз
Клинические рекомендации при синдроме Гудпасчера зависят от типа недуга, а также от индивидуальных свойств пациента. В целом они основаны на угнетении патологической реакции иммунной системы на собственные ткани. Существует несколько различных видов медикаментов, которые используются в качестве основного лечения заболевания:
- Кортикостероиды представляют собой обширную группу препаратов. Они обладают выраженным противовоспалительным действием за счет угнетения защитных сил организма. К данным средствам относят «Метипред» и «Дексаметазон». Эти вещества известны выраженным терапевтическим действием. Однако препараты имеют множество противопоказаний и побочных эффектов. В связи с этим перед их применением требуется комплексное обследование пациента.
- Иммуносупрессивным действием обладают и цитостатики. Наиболее часто эти средства используются при лечении онкологических проблем, но активно назначаются и для борьбы с ревматоидными поражениями. К препаратам данной группы относятся такие вещества, как «Циклофосфамид» и «Азатиоприн».

Большое значение в борьбе с недугом имеет и симптоматическая терапия. Она сводится к назначению антибиотиков, которые требуются для предотвращения вторичного инфицирования на фоне угнетения иммунных сил организма. При развитии тяжелой степени анемии прибегают к проведению переливаний крови. Для удаления из организма патологических антител к базальной мембране сосудов используется плазмаферез, обладающий выраженным терапевтическим эффектом. При формировании почечной недостаточности, угрожающей жизни пациента, рекомендации сводятся к гемодиализу. В ряде случаев прибегают к трансплантации пораженного органа.
Прогноз при синдроме Гудпасчера, как правило, неблагоприятный. Это связано со стремительным развитием болезни и поражением жизненно важных систем. В большинстве случаев пациенты погибают от последствий почечной недостаточности, а также вследствие развития сильного легочного кровотечения.
По статистике, собранной в Соединенных Штатах Америки, заболевание диагностируется у 1 пациента из миллиона в течение года. Из всех случаев регистрации гломерулонефрита у взрослых синдром Гудпасчера выявляется у 5% пострадавших. При этом из всех образцов тканей почек, взятых при помощи биопсии, данная аутоиммунная проблема составляет лишь 1–2%. При этом в случае диагностики стремительно прогрессирующей недостаточности функций клубочкового аппарата соотношение меняется. У 20% взрослых пациентов и у 10% детей с быстро усугубляющимся гломерулонефритом выявлен синдром Гудпасчера.
Прогноз при недуге неблагоприятный, хотя при наличии своевременного лечения 90% человек переносят острую фазу развития болезни. Однако двухлетняя выживаемость при этом достигает лишь 50%. Летальный исход обусловлен терминальной стадией почечной недостаточности, риск которой при синдроме Гудпасчера крайне высок. 15% случаев выявления выраженного нарушения работы мочевыделительной системы в США представляют собой проявление этого расстройства. Недугу подвержены люди различной расы и пола, при этом среди детей минимальный зарегистрированный возраст выявления аутоиммунной проблемы составляет 11 месяцев.
Рекомендации по профилактике
Поскольку точный патогенез недуга на сегодняшний день неизвестен, то и алгоритма его предупреждения не разработано. Общие принципы сводятся к своевременному обращению к врачу. Хотя для синдрома и характерно стремительное развитие, с ним намного проще бороться на ранних этапах возникновения. Поскольку триггеры в формировании недуга – вирусные и бактериальные инфекции, к числу профилактических рекомендаций относится недопущение заражения. Для этого требуется придерживаться принципов здорового образа жизни, что означает правильное и сбалансированное питание, умеренные физические нагрузки и отказ от вредных привычек. Такой подход поддерживает естественную работу иммунитета, являясь основным условием предупреждения проблемы.
Отзывы о лечении
Руслан, 36 лет, г. Москва
У дочери выявили синдром Гудпасчера. Врачи сказали, что у нее постепенно отказывают почки. Позднее возникло еще и воспаление легких. Ее госпитализировали, делали капельницы, проводили плазмаферез и переливание крови. Дочь пролежала в больнице две недели, была в тяжелом состоянии. Несмотря на приложенные усилия, спасти ребенка не удалось.
Елена, 24 года, г. Омск
Начался сильный кашель с кровью. Во время обследования врачи выявили синдром Гудпасчера. Меня поместили в отделение интенсивной терапии, где проводили плазмаферез. Состояние стабилизировалось, поэтому лечусь амбулаторно. Несмотря на то, что стала чувствовать себя лучше, врачи не дают никаких гарантий.
Синдром Гудпасчера: причины, симптомы, диагностика, лечение

Весь контент iLive проверяется медицинскими экспертами, чтобы обеспечить максимально возможную точность и соответствие фактам.
У нас есть строгие правила по выбору источников информации и мы ссылаемся только на авторитетные сайты, академические исследовательские институты и, по возможности, доказанные медицинские исследования. Обратите внимание, что цифры в скобках ([1], [2] и т. д.) являются интерактивными ссылками на такие исследования.
Если вы считаете, что какой-либо из наших материалов является неточным, устаревшим или иным образом сомнительным, выберите его и нажмите Ctrl + Enter.

Синдром Гудпасчера – аутоиммунный синдром, включающий альвеолярное легочное кровотечение и гломерулонефрит, вызванный циркулирующими анти-GBM-антителами. Синдром Гудпасчера чаще всего развивается у людей с наследственной предрасположенностью, которые курят сигареты, но возможными дополнительными факторами являются вдыхание углеводорода и вирусные инфекции дыхательных путей. Симптомы синдрома Гудпасчера включают одышку, кашель, усталость, кровохарканье и/или гематурию. Синдром Гудпасчера подозревается у пациентов с кровохарканьем или гематурией и подтверждается наличием анти-GВМ-антител в крови. Лечение синдрома Гудпасчера включает плазмаферез, глюкокортикоиды и иммунодепрессанты типа циклофосфамида. Прогноз благоприятен, если лечение начато до развития дыхательной или почечной недостаточности.
Синдром Гудпасчера впервые описано Гудпасчером в 1919 году. Синдром Гудпасчера представляет собой комбинацию гломерулонефрита и альвеолярного кровотечения в присутствии анти-GВМ-антител. Синдром Гудпасчера чаще всего проявляется сочетанием диффузного альвеолярного кровотечения и гломерулонефрита, но иногда вызывает изолированный гломерулонефрит (10-20 %) или поражение легких (10 %). Мужчины болеют чаще, чем женщины.

[1], [2], [3], [4], [5]
Что вызывает синдром Гудпасчера?
Причина заболевания точно не установлена. Предполагается генетическая предрасположенность к синдрому Гудпасчера, ее маркером считают наличие HLA-DRW2. Существует точка зрения о возможной роли перенесенной вирусной инфекции (вирус гепатита А и др. вирусные заболевания), производственных вредностей, лекарственных препаратов (прежде всего D-пеницилламина).
Основой патогенеза синдрома Гудпасчера является образование аутоантител к базальным мембранам капилляров клубочков почек и альвеол. Эти антитела относятся к классу IgG, они связываются с антителами базальных мембран в присутствии С3-компонента комплемента с последующим развитием иммунного воспаления почек и альвеол легких.
Анти-GВМ-антитела направлены против неколлагенового (NC-1) домена аЗ цепи коллагена IV типа, который в наиболее высокой концентрации находится в базальных мембранах почечных и легочных капилляров. Воздействие экологических факторов – курения, вирусных ОРЗ и вдыхания гидрокарбонатных взвесей (более часто) – и, менее часто, пневмонии активизирует презентацию антигенов альвеолярных капилляров циркулирующим антителам у людей с наследственной предрасположенностью (наиболее часто это носители HLA-DRwl5, – DR4 и – DRB1 аллелей). Циркулирующие анти-GВМ-антитела связываются с базальными мембранами, фиксируют комплемент и вызывают клеточный воспалительный ответ, приводящий к развитию гломерулонефрита и/или легочного капиллярита.
Вероятно, существует определенная общность ауто-антигенов базальной мембраны капилляров клубочков почек и альвеол. Аутоантиген формируется под влиянием повреждающего действия этиологического фактора. Неизвестный этиологический фактор повреждает и модифицирует структуру базальных мембран почек и легких. Экскреция образовавшихся продуктов деградации базальных мембран клубочков почек при их поражении замедляется и уменьшается, что, естественно, создает предпосылки для развития аутоиммунного поражения почек и легких До сих пор окончательно неизвестно, какой компонент базальной мембраны становится ауто-антигеном. В настоящее время предполагается, что это внутренний структурный компонент базальной мембраны клубочка почки а3-цепь коллагена 4 типа.
Сформировавшиеся иммунные комплексы откладываются вдоль базальных мембран капилляров клубочков, что приводит к развитию иммуновоспалительного процесса в почечном клубочке (гломерулонефрит) и альвеолах (альвеолит). Основными клетками, принимающими участие в развитии этого иммунного воспаления, являются Т-лимфоциты, моноциты, эндотелиоциты, полиморфноядерные лейкоциты, альвеолярные макрофаги. Взаимодействие между ними обеспечивается молекулярными медиаторами, цитокинами (факторы роста – тромбоцитарный, инсулиноподобный, b-трансформирующий; интерлейкин-1, фактор некроза опухоли и др ). Большую роль в развитии иммунного воспаления играют метаболиты арахидоновой кислоты, свободные радикалы кислорода, протеолитические ферменты, адгезивные молекулы.
В развитии альвеолита при синдроме Гудпасчера огромное значение имеет активация альвеолярных макрофагов. В активированном состоянии они выделяют около 40 цитокинов. Цитокины I группы (хемотаксины, лейкотриены, интерлейкин-8) усиливают поступление полиморфноядерных лейкоцитов в легкие. Цитокины II группы (факторы роста – тромбоцитарный, макрофагальный) способствуют перемещению в легкие фибробластов. Альвеолярные макрофаги продуцируют также активные формы кислорода, протеазы, повреждающие легочную ткань.