Острый лейкоз (лейкемия)
Острый лейкоз – тяжелая патология кроветворной системы, при которой в крови появляется большое количество бластных (незрелых) лейкоцитов. Злокачественная мутация стволовой клетки в костном мозге приводит к развитию опухоли. Видоизменившийся кроветворный орган производит бластные клетки, которые с течением времени все больше вытесняют нормальные клетки. У пациента снижается иммунитет, результатом становятся воспалительные процессы, инфекции, кровотечения, состояние больного быстро ухудшается. Острый лейкоз крови никогда не переходит в хроническую фазу. Заболевание характеризуется стремительным течением и высокой агрессивностью злокачественных клеток.
Согласно общепринятой классификации, острые лейкозы подразделяют на лимфобластные, нелимфобластные и недифференцированные, в зависимости от типа патологически измененных клеток.
- В-клеточные пре-формы;
- зрелый В-клеточный лейкоз;
- Т-клеточные пре-формы;
- кортикальная Т-клеточная форма;
- зрелый Т-клеточный лейкоз.
Эти формы наиболее часто развиваются у детей и у людей старшего возраста. Среди детских онкозаболеваний острые лейкозы занимают первое место по частоте.
Нелимфобластные острые лейкозы:
- миелобластный;
- миеломонобластный и монобластный;
- мегакариобластный;
- эритробластный.
Симптомы
У всех видов острых лейкозов симптомы практически одинаковы и на начальном этапе выражены довольно слабо. Специфических признаков нет, заболевание может разворачиваться постепенно или, напротив, внезапно и бурно. Наиболее типичными проявлениями становятся:

- повышение температуры, лихорадка;
- повышенное выделение пота, особенно по ночам;
- резкий упадок сил, сонливость;
- бледность кожных покровов;
- увеличение размеров лимфоузлов, печени, селезенки;
- плохо заживающие ранки и ссадины на коже и слизистых оболочках;
- легко образующиеся синяки, гематомы, кровотечения;
- обширные кровоподтеки на коже;
- частые инфекции и воспаления.
На начальной стадии заболевание легко принять за грипп или простуду. Если недомогание не прекращается в течение двух или более недель, обязательно следует посетить онколога.
Причины и факторы риска
Единственной причиной развития острого лейкоза является злокачественное изменение гена стволовой клетки костного мозга, запускающей кроветворный процесс. Бесконтрольное размножение мутировавших опухолевых клеток приводит к нарушению кроветворения и постепенному вытеснению здоровых клеток злокачественными. Среди факторов, оказывающих негативное влияние на костный мозг и кроветворную систему, наиболее значительными являются:
- высокие дозы радиоактивного излучения;
- некоторые виды химических соединений;
- Т-лимфотропные вирусы;
- курение табака, другие загрязнения воздуха;
- унаследованная предрасположенность к онкопатологиям;
- иммунодефицитные состояния.
Перечисленные факторы характеризуются недостаточной активностью иммунной системы, которая не успевает распознать и уничтожить злокачественные клетки сразу после их появления.
Стадии
Классификация острого лейкоза разделяет течение болезни на три стадии:
- начальную, со слабо выраженной неспецифической симптоматикой;
- развернутую, состоящую из фаз дебюта (атаки), ремиссии и рецидива либо выздоровления;
- терминальную, во время которой здоровые клетки практически перестают продуцироваться кроветворной системой, что приводит к резкому ухудшению состояния больного.
Заболевание обнаруживают во время дебюта развернутой стадии острого лейкоза, когда костный мозг начинает активно продуцировать бластные клетки. Активные усилия онкологов-гематологов приводят к снижению их количества в крови больного до 5% или ниже. Если это состояние сохраняется в течение пяти лет, то ремиссия считается полной, а пациент – вылеченным. При неполной ремиссии количество бластных клеток в крови через некоторое время вновь возрастает более 5%.
Диагностика
Для постановки диагноза и определения типа заболевания требуются лабораторные исследования.
Общий анализ крови с подсчетом лейкоцитарной формулы для первичной диагностики патологии.
Биохимический анализ крови, чтобы выявить ухудшения в работе печени и почек.
Биопсия костного мозга для последующего изучения (обычно берется из подвздошной кости).
Гистологическое исследование биоптата. Необходимо для выявления злокачественных клеток.
Цитохимический анализ биоптата. Определяются специфические ферменты, характерные для тех или иных бластов.
Иммунофенотипический анализ. Определение поверхностных антигенов позволяет точно установить вид острого лейкоза.
Цитогенетический анализ. Выявляет повреждения хромосом, что позволяет точно определить разновидность заболевания.
Молекулярно-генетический анализ. Проводится в случаях, когда другие методы не дают однозначного результата.
УЗИ органов брюшины. Подтверждение увеличения размеров печени и селезенки, выявление метастазов в лимфоузлах и других внутренних органах.
Рентген грудной клетки. Выявление увеличенных лимфоузлов, воспалительного процесса в легких.
В дальнейшем могут понадобиться другие диагностические исследования для уточнения диагноза и для наблюдения за изменением состояния пациента.
Вы можете бесплатно получить медицинскую помощь в АО «Медицина» (клиника академика Ройтберга) по программе по программе Государственных гарантий ОМС (Обязательного медицинского страхования) и ВМП (высокотехнологичной медицинской помощи).
Чтобы узнать подробности, позвоните, пожалуйста, по телефону +7 (495) 775-73-60 , или можете прочитать более подробно здесь…
Лечение
В настоящее время существует множество способов лечения острого лейкоза.
Химиотерапия – основной метод, который заключается в применении специфических медикаментов, уничтожающих злокачественные клетки. Как правило, онкологи-химиотерапевты применяют многокомпонентные схемы, подбирая препараты в зависимости от типа лейкозных клеток и индивидуальных особенностей организма. Схема терапии состоит из четырех основных этапов: индукции – основного ударного воздействия, консолидации – закрепления результата, реиндукции – повторной индукции для уничтожения «спящих» лейкозных очагов, и в качестве завершающего этапа – поддерживающей терапии с невысокими дозами цитостатиков.
Лучевая терапия, как правило, назначается перед пересадкой костного мозга для максимального уничтожения лейкозных клеток.
В перечне клинических рекомендаций при остром лейкозе важнейшее место занимает исключение любых инфекций во время лечения. Перед началом курса пациент должен избавиться от кариозных зубов, пролечить инфекции дыхательных путей и т.д. Во время лечения он находится в стационаре, в котором поддерживается жесткий асептический режим, исключающий случайное инфицирование.
Прогнозы
Несколько десятилетий назад диагностированный острый лейкоз, по сути, являлся приговором. В настоящее время ситуация существенно улучшилась, применение новых, эффективных препаратов позволяет добиваться излечения более чем половины пациентов. При своевременно начатом лечении полная ремиссия наступает у 45-80% больных. Лучшие показатели – у детей до 10 лет, среди которых полностью выздоравливают до 86% пациентов, худшие – у пожилых людей, пятилетняя выживаемость которых не превышает 30%.
Профилактика
Специальных мер по профилактике острого лейкоза в настоящее время не существует. Чтобы снизить риски заболевания, необходимо придерживаться здорового образа жизни, отказаться от курения, соблюдать требования безопасности при работе на вредном производстве.
Реабилитация
Восстановление после тяжелого химиотерапевтического воздействия направлено на снижение риска осложнений острого лейкоза, и в первую очередь – на восстановление функций иммунной системы при помощи:
- общеукрепляющего лечения – витаминных комплексов, препаратов железа, иммуномодуляторов;
- восстановления микрофлоры кишечника при помощи пробиотиков;
- дезинтоксикационных процедур;
- улучшения сна, укрепления нервной системы;
- психотерапии.
Диагностика и лечение острого лейкоза в Москве
Если у вас обнаружены симптомы острого лейкоза, обратитесь в клинику «Медицина». Мы предлагаем своим пациентам;
- точную и быструю диагностику при помощи самого современного оборудования;
- лечение у специалистов высшей квалификации – онкологов, гематологов, химиотерапевтов;
- пребывание в комфортабельном, превосходно оборудованном стационаре;
- медицинский сервис мирового уровня.
Позвоните нам, чтобы записаться на первичную консультацию к одному из лучших онкологов Москвы.
Вопросы и ответы
Сколько живут с острым лейкозом крови?
При отсутствии лечения летальный исход наступает в течение 1-2 лет после диагностирования острого лейкоза. Современные методы и эффективные препараты позволяют добиваться полной ремиссии у 80% больных, в зависимости от их возраста, текущего состояния, стадии процесса и других факторов. Более половины пациентов по окончании лечения проживают свыше 10 лет.
Как проявляется лейкоз?
Внешние проявления заболевания на начальной стадии напоминают симптомы обычной простуды, поэтому на них часто не обращают внимания. Если в течение двух недель не снижается повышенная температура, не проходит слабость, недомогание, потливость и другие «простудные» ощущения – необходимо как можно скорее обратиться к онкологу для обследования.
Можно ли вылечить острый лейкоз?
При остром лейкозе своевременное начало лечения во много раз повышает шансы больного на выздоровление. Поэтому при обнаружении беспокоящих признаков следует посетить онколога, ведь они могут оказаться симптомами тяжелой и опасной, стремительно развивающейся болезни. В этом случае нельзя терять время, ведь каждый день снижает шансы на успех лечения.
Внимание!
Вы можете бесплатно вылечить это заболевание и получить медицинскую помощь в АО «Медицина» (клиника академика Ройтберга) по программе Государственных гарантий ОМС (Обязательного медицинского страхования) и ВМП (выскокотехнологичной медицинской помощи).
Чтобы узнать подробности, позвоните, пожалуйста, по телефону +7(495) 775-73-60, или на странице ВМП по ОМС
Острый лейкоз (острая лейкемия)

Острым лейкозом называют онкозаболевание крови и кроветворного органа — красного костного мозга, при котором нормальные лейкоциты постепенно вытесняются незрелыми (бластными) клетками, неспособными выполнять свою функцию. В результате у больного развиваются воспаления и кровотечения внутренних органов, которые существенно ухудшают его состояние, резко снижается иммунитет, поражается нервная система. При отсутствии квалифицированной медицинской помощи неизбежно наступает неблагоприятный исход. Заболевание характеризуется высокой агрессивностью: мутировавшие клетки быстро распространяются по организму, а их число растёт с высокой скоростью.
Виды заболевания
Онкогематологи, в зависимости от характера патологии клеток, выделяют две основные разновидности острого лейкоза крови.
- Лимфобластный. Составляет примерно 15-20% случаев. Вначале злокачественные клетки поражают костный мозг, затем распространяются в лимфоузлы, вилочковую железу и селезёнку и далее по всему организму. Характерная особенность — мутировавшие клетки лишены липидов, эстеразы, пероксидазы. Наиболее часто развивается у детей в возрасте от года до шести лет и у взрослых после сорока лет. В свою очередь, подразделяется на два вида: В-форму с благоприятным прогнозом для трети взрослых и двух третей заболевших детей, и Т-форму с крайне тяжёлым течением и печальным исходом.
- Миелобластный. Заболевание, как правило, развивается во взрослом возрасте, ему одинаково подвержены мужчины и женщины. Перспективы лечения достаточно оптимистичны: частичной ремиссии удаётся добиться для 80% больных, полное выздоровление наступает не менее чем у 20%.
Полная классификация острых лейкозов включает множество подвидов, которые различаются по морфологическим, генетическим и другим признакам, требующих специфического лечения.
Симптомы
Первые признаки, по которым можно заподозрить начало заболевания, одинаковы для всех его форм.
- Заметная потеря веса, не связанная с ограничением в пище или физическими нагрузками.
- Усталость, ухудшение общего самочувствия.
- Постоянная слабость, апатия, сонливость.
- Ощущение тяжести после еды, часто концентрирующееся в области левого подреберья и не зависящее от количества и калорийности съеденного.
- Частые инфекционные заболевания.
- Повышенное выделение пота, особенно по ночам.
- Повышенная температура тела.
По мере роста злокачественных клеток в крови появляются более выраженные симптомы острого лейкоза.
- Бледность кожных покровов, одышка из-за недостатка кислорода, переносимого кровью, анемия.
- Частые кровотечения из носа и дёсен, кровоподтёки на коже и слизистых, у женщин — обильные месячные.
- Нарушение функций поражённых внутренних органов со своими специфическими проявлениями.
- Сильные боли в костях и суставах.
- Увеличение в размерах селезёнки и печени.
- Постоянные отёки рук и лица.
Клинические признаки не дифференцируются в соответствии с классификацией острого лейкоза, поэтому определить форму болезни можно только при помощи лабораторных исследований.
Причины и факторы риска
До сих пор точно не установлены этиологические факторы, которые неизбежно становятся «спусковым крючком» для злокачественной мутации клеток. Однако риски развития острого лейкоза существенно повышаются при:
- радиационном облучении, которому подвергается человек;
- заражении определёнными вирусами, угнетающими иммунную систему (болезнь Эпштейна-Барра, Т-лимфотропный вирус и др.);
- неблагоприятной наследственности;
- курении табака;
- длительном воздействии некоторых химических соединений, в том числе лекарственных препаратов;
- стрессах, депрессивных состояниях;
- загрязнении окружающей среды.
Стадии
Онкогематологи выделяют следующие стадии острого лейкоза.
- Начальная. Протекает скрытно, длится от нескольких месяцев до нескольких лет. Диагностируется только при исследовании костного мозга, так как анализы крови показывают лишь незначительные отклонения по количеству лейкоцитов, а симптомы отсутствуют.
- Развёрнутая. В крови резко возрастает количество незрелых клеток, что приводит к ухудшению самочувствия и появлению начальных симптомов болезни.
- Ремиссия. Проявления онкопатологии уменьшаются, тем не менее, в костном мозге остаётся определённое количество бластных клеток (при полной ремиссии — не более 5%).
- Рецидив. Количество незрелых клеток в костном мозге и в крови пациента увеличивается, а его состояние ухудшается.
- Терминальная. Самая тяжёлая стадия болезни, для которой характерны многочисленные осложнения острого лейкоза: поражаются жизненно важные внутренние органы, происходят обширные кровотечения, изъязвление и некротизация тканей.
Диагностика
Пациенту с симптомами, напоминающими острый лейкоз, назначают:
- анализы крови — общий, биохимический, коагулограмма;
- изъятие костного мозга из подвздошной кости или грудины с последующим проведением цитохимического анализа, иммунофенотипирования, морфологического анализа клеток;
- пункция костного мозга и ликвора для цитологического и гистологического исследования;
- инструментальные исследования внутренних органов — УЗИ, рентгенография, КТ, МРТ для оценки степени их поражения злокачественными клетками;
- консультации невролога, отоларинголога, офтальмолога и других специалистов.
Лечение
Поскольку в перечень наиболее агрессивных злокачественных онкозаболеваний входит острый лейкоз, лечение должно начаться сразу после постановки диагноза. Пациента помещают в онкогематологический стационар в палату со специальной вентиляцией для удаления патогенной микрофлоры. Основным методом, как правило, является химиотерапия, которая подкрепляется переливанием компонентов крови, дезинтоксикационной терапией, профилактикой инфекций. Схема лечения состоит из основных этапов:
- индукция ремиссии — воздействие химиопрепаратов, уничтожающих бластные клетки, чтобы достигнуть максимально возможной ремиссии;
- консолидация — закрепление достигнутых результатов;
- предупреждение рецидива — исключение возврата заболевания.
При определённых формах заболевания хороший эффект даёт трансплантация стволовых клеток костного мозга, выполняемая после уничтожения бластов с помощью химиопрепаратов и лучевой терапии.
Первый этап лечения занимает от 4 до 6 недель, в это время пациент получает массированную терапию. На этапе консолидации проводится два или три курса лечения, после чего в течение нескольких лет продолжаются поддерживающие мероприятия, которые необходимы, чтобы исключить рецидивы. Полная ремиссия достигается при уничтожении клона патологических клеток и восстановлении нормального кроветворного процесса.
Прогнозы
Современные методы лечения позволяют перевести в фазу длительной ремиссии до 80% больных, из них до 30% случаев составляет полное выздоровление. Чем раньше обнаружено заболевание, тем более благоприятен прогноз. Тем не менее, даже для пациентов, у которых рак крови диагностирован в терминальной стадии, остаются шансы на излечение.
Профилактика
Чтобы снизить вероятность мутации кроветворных клеток, необходимо придерживаться здорового образа жизни, исключить курение табака, избегать стрессов и депрессивных состояний. Людям с отягощённой наследственностью, подвергавшимся облучению или часто контактирующим с опасными химическими соединениями, в целях профилактики острого лейкоза следует тщательно следить за здоровьем и регулярно консультироваться с онкологом для своевременного обнаружения болезни.
Реабилитация
В перечень клинических рекомендаций при остром лейкозе в период реабилитации входят:
- мероприятия по повышению иммунитета;
- сбалансированное питание;
- дезинтоксикационная терапия;
- восстановление кишечной микрофлоры;
- антистрессовая психотерапия;
- улучшение качества сна.
В период восстановления важно выполнять все назначения лечащего врача-онколога, вовремя и полностью проходить рекомендованные лечебные курсы.
Диагностика и лечение острого лейкоза в Москве
Клиника Института ядерной медицины выполняет качественную диагностику острого лейкоза с использованием современных медицинских приборов и оборудования. При подтверждении диагноза квалифицированные онкогематологи проводят надлежащее лечение, отвечающее самым высоким стандартам, принятым в современной мировой практике.
Вопросы и ответы
Острый лейкоз крови: сколько живут с этим заболеванием?
Шансы прожить пять лет и более для детей существенно выше, чем для взрослых и составляют 75-80%. У взрослых этот показатель достигает 30%, но в некоторых клиниках превышает 50%. Длительность жизни зависит от формы заболевания: при остром лимфобластном лейкозе она составляет 2-3 года, а с миелоидной формой пациенты живут, в среднем, около 6 лет.
Как проявляется лейкоз?
Коварство этого заболевания заключается в отсутствии выраженной симптоматики. Пациент ощущает ухудшение своего состояния, однако считает, что причина заключается в усталости, сезонной простуде и т. д. Обнаружить и диагностировать острый лейкоз на ранней стадии болезни могут только онкологи-гематологи, которые используют специфические методики и оборудование.
Можно ли вылечить острый лейкоз?
Как и при любом онкозаболевании, наиболее благоприятны прогнозы при максимально раннем обнаружении острого лейкоза и незамедлительном начале лечения. Возможность выздоровления существует для каждого пациента, независимо от стадии и формы болезни, поэтому необходимо не опускать руки, а обращаться в клинику ИЯМ, где вам окажут квалифицированную помощь на самом высоком современном уровне.
Как распознать лейкоз по анализу крови?
Врач-гематолог, профессор кафедры онкологии, гематологии и лучевой терапии РНИМУ им. Н. И. Пирогова Минздрава России, доктор медицинских наук Сергей Семочкин рассказал: можно ли распознать острый лимфобластный лейкоз (ОЛЛ) на ранней стадии и поставить диагноз по анализу крови; объяснил, как лечат ОЛЛ и кому показана трансплантация костного мозга (ТКМ).
Каковы ранние симптомы острого лимфобластного лейкоза? Можно ли их увидеть и распознать ОЛЛ?
В данном случае все достаточно просто, потому что слово «острый» означает, что заболевание внезапное и зачастую симптомы очень выразительные. Самый частый симптом — это лихорадка, т.е. повышение температуры тела. Лихорадка может быть как субфебрильной, так и ярко выраженной, до 39 градусов. Появятся изменения, связанные с поражением костного мозга. Снижение гемоглобина приведет к слабости и быстрой утомляемости. Могут увеличиться лимфатические узлы, появиться дискомфорт в брюшной полости за счет того, что увеличиваются размеры печени и селезенки. Могут быть проявления кровоточивости — даже во время чистки зубов. У некоторых пациентов ОЛЛ может начаться с неврологических проявлений – головных болей, головокружения и прочих проблем. Симптоматика обширная, но в данном случае она является достаточно острой, внезапно возникшей.
Можно ли поставить диагноз по анализу крови? Что он покажет?
Как правило, в анализе крови есть ярко выраженные показатели: изменены ростки кроветворения, количество лейкоцитов выходит за пределы нормы — может упасть ниже нормальных значений, а может стать запредельно огромным. Мне встречались пациенты, у которых количество лейкоцитов при норме от 4 до 9 тысяч повышалось до 200 тысяч на мкл. Тромбоциты тоже в ряде случаев очень сильно снижены, но главное – изменение количества лейкоцитов. Очень важным маркером является выход опухолевых клеток в кровь, когда в крови появляются незрелые ранние клетки, которые называют бластными. Если в анализе крови выявили бластные клетки, то это, скорее всего, либо острый лейкоз, либо миелодиспластический синдром.
Как пациент попадает к гематологу?
Анализ крови с характерными изменениями — повод для немедленного вызова скорой помощи и госпитализации пациента в профильный стационар. При лечении детей и подростков у онкогематолога, как правило, есть один-два дня ни диагностику, лечение необходимо начинать, как можно раньше. В диагностику входит повторный анализ крови, затем – верификация диагноза, для которой проводят биопсию костного мозга. У маленьких детей ее проводят под общей анестезией, у взрослых — под местной. С помощь небольшой иглы делаю прокол грудины или подвздошной кости. У детей пункцию грудины не делают. Полученный образец костного мозга, который выглядит как обычная пробирка с кровью, отправят в лабораторию, где для подтверждения диагноза проведут целый спектр исследований. Главный критерий – увеличение количества бластных клеток. Только по внешнему виду и по количеству бластных клеток определить вариант лейкоза – невозможно. Еще в 1913 году установили, что есть лимфоидный, а есть миелоидный вариант лейкоза. Для верификации применяются специальные лабораторные методы: иммунологические и химические. Существует специальный прибор – проточный цитометр, с помощью которого определяют маркеры, характеризующие данный тип клеток. Для определения подвида острого лейкоза, применяют целый спектр генетических исследований, чтобы выйти на более целевую терапию у этих пациентов.
Каковы причины возникновения ОЛЛ? Существует мнение, что этот вид лейкоза очень сильно взаимосвязан с экологическими проблемами, передается по наследству и часто возникает у тех, кто уже переболел каким-то онкологическим заболеванием. Правда это или нет?
Истинную причину возникновения лейкоза у взрослых можно выявить только в 5% случаев, в 95% совершенно непонятно, что там к чему привело. У детей все несколько интересней.
Как возникает лейкоз? В генетическом материале клетки возникает некая первичная мутация, которая сама по себе далеко не всегда приводит к лейкозу. В дальнейшем к этой мутации присоединяются другие, и когда болезнь все же возникает, в клетке накоплено уже много молекулярных событий, сочетание которых привело возникновению заболевания. Пик острого лимфобластного лейкоза приходится на детей от двух до четырех лет, потом заболеваемость падает. Следующий пик приходится на 18-29 лет, потом снова спад. После 60 лет — опять небольшой рост.
У части детей раннего возраста прослеживается некая врожденная составляющая этой проблемы. Встречаются случаи ОЛЛ у плода или новорожденного, когда ребенок рождается уже с заболеванием, либо заболевает в течение первого года жизни. Исследования пуповинной крови показали, что у новорожденных встречаются лейкемические поломки, врожденные мутации, которые могут привести к возникновению лейкоза. И мутацию эту вызывает наследственный фактор, сработавший во время внутриутробного развития. По разным данным, общее количество таких младенцев составляет от 1 до 5%. Дальше многое зависит от инфекционной обстановки, сложившейся вокруг ребенка. Многочисленные инфекции, перенесенные в детстве, способствуют формированию нормальной иммунной системы, которая нейтрализует наследственный фактор.
Если говорить про экологические проблемы, то с ними четкой связи не выявлено.
Влияет ли УФ-излучение, СВЧ, солнечные лучи, радиация?
В Хиросиме и Нагасаки повышенная заболеваемость держалась около 12 лет. После Чернобыля у многих пострадала щитовидная железа, но заболеваемость лейкозами не выросла. Все зависит от типа изотопов попавших в окружающую среду. В Фукусиме тоже этого не случилось, потому что концентрация радиоактивных веществ сильно разбавилась морской водой.
Вред ультрафиолета научно доказан только в отношении меланомы. Четкой связи с ОЛЛ нет. Своим бывшим пациентам мы не разрешаем посещать солярий и не рекомендуем загорать, потому что хотя связь и не доказана, совсем исключать этот фактор тоже нельзя.
Если говорить об СВЧ-излучении, домашние микроволновые печи абсолютно безопасны.
Как лечат ОЛЛ? Что ждет пациента?
Концепция лечения ОЛЛ, которая до сих поре лежит в основе протоколов лечения ОЛЛ, была разработана американским педиатром Дональдом Пинкелем еще в 1962 году. Она включает в себя четыре этапа: индукция ремиссии, консолидация, воздействие на центральную нервную систему и длительный этап поддерживающей терапии на протяжении двух-трех лет. Во всем мире проводится лечение по клиническим протоколам, разработанным в результате кооперированных исследований. Согласно некоторым работам, строгое следование протоколам повышает выживаемость пациентов на 15-20% по сравнению с индивидуализированным лечением. В протоколе прописаны все действия: от первого дня до последнего. В нем есть указания, как и в какой момент оценивать возникающие осложнение и что с ними делать. В России два центра, активно ведущих такие протоколы. Центр им. Дмитрия Рогачева, где Александр Исаакович Карачунский в течение многих лет, с начала 1990-х, ведет серию протоколов «Москва — Берлин». Каждые пять лет дизайн протоколов пересматривают, чтобы улучшить лечение отдельных категорий пациентов. уже в течение многих лет с начала 90-х годов серию протоколов Москва-Берлин. Каждые пять лет меняется дизайн протоколов, направленных на улучшение лечения отдельных категорий пациентов. Во взрослой практике — это НМИЦ гематологии, где ведут кооперированные исследования по острому лимфобластному лейкозу у взрослых.
В каких случаях показана трансплантация костного мозга (ТКМ)?
В отличие от острого миелоидного лейкоза, показаний к аллогенной (от донора) ТКМ меньше. Ее назначают пациентам, которые не достигли ремиссии в указанные протоколом сроки или имеют неблагоприятный цитогенетический вариант заболевания. В детской практике выздоравливают более 90% детей, и примерно 15-20% являются кандидатами для аллогенной ТКМ. У взрослых процент пациентов нуждающихся в трансплантации несколько выше, за счет того, что генетических операций высокого риска становится намного больше и ответ на стандартное лечение хуже. Когда мы обсуждали хронический миелолейкоз, там фигурировала филадельфийская хромосома — транслокация (9;22). При ОЛЛ это абсолютно негативный фактор прогноза. У детей такая мутация встречается меньше чем в 5% случаев, у людей старше 50-60 лет примерно половина В-линейных ОЛЛ будет с филадельфийской хромосомой. В отличие от хронического миелолейкоза, применение ингибиторов тирозинкиназы при остром лимфобластном лейкозе не столь успешно. Вот поэтому во взрослой практике ТКМ необходимо проводить примерно 30% пациентов. Возрастной порог для аллогенной ТКМ — в районе 55 лет, это разумно.
Как часто случаются рецидивы с ОЛЛ?
Если мы говорим про взрослых людей, то рецидивы случаются почти в 40% случаев. Бывают ранние рецидивы, которые случаются прямо на терапии. В таком случае необходимо менять лечение, делать его более интенсивным и тяжелым. В таких случаях, как правило, показана ТКМ. Поздний рецидив может случиться и через 20 лет. К сожалению мы не можем убрать причину, которая вызывает это заболевание — оно может вернуться.
Можно ли планировать беременность после ОЛЛ?
Длительная химиотерапия нарушает фертильность, поэтому лучше провести криоконсервацию спермы/яйцеклетки, а еще лучше эмбриона — это более надежный способ. У мужчин, как правило, серьезно нарушается сперматогенез, но у женщин дело обстоит несколько лучше. Вероятность забеременеть и выносить здорового ребенка высока. Если прошло не менее пяти лет в ремиссии, никаких ограничений нет.
Может ли беременность быть провоцирующим фактором для рецидива?
Скорее, нет. Это не такое частое явление, как при некоторых других заболеваниях, где беременность действительно может стать провоцирующим фактором.
Передается ли ОЛЛ по наследству?
Лимфобластный лейкоз – редкое заболевание, поэтому вероятность того, что он случится у ребенка, рожденного от родителей после ОЛЛ, крайне мала.
Как будут лечить ОЛЛ в будущем?
Представляется, что в основе лечения онкологических заболеваний в будущем станет активация собственного иммунитета. Нам необходимо настроить иммунную систему таким образом, чтобы она распознавала и убирала раковые клетки. Сейчас мы находимся на раннем этапе развития CAR-T-терапии, но через какое-то время технологии настолько усовершенствуются, что, скорее всего, она станет одним из основных методов терапии при целом ряде онкогематологических заболеваний. Суть метода заключается в том, что у пациента собирают его собственные Т-лимфоциты и отправляют в специальную лабораторию. Эта лаборатория может быть в другом городе, стране — не важно. В лаборатории эти Т-лимфоциты перепрограммируются: в них появляется информация об опухолевых клетках, присутствующих в организме пациента. После перепрограммирования Т-лимфоциты вводят обратно пациенту, она находят раковые клетки и возникает ремиссия. Основные проблемы – создать качественный процесс распознавания и разработать стандартные протоколы лечения.
Много вопросов возникает в понимания биологии заболевания, потому как каждый конкретный случай весьма индивидуален. Мы знакомы только с грубыми поломками, но каждая отдельная поломка провоцирует различное течение болезни. Мы уже сейчас можем полностью секвенировать геном опухолевой клетки и главное научиться понимать, что в патогенезе является ключевым и как на это можно воздействовать, тогда мы ближе подойдем к полному излечению болезни. За этим будущее.
Лейкоз
Информацию из данного раздела нельзя использовать для самодиагностики и самолечения. В случае боли или иного обострения заболевания диагностические исследования должен назначать только лечащий врач. Для постановки диагноза и правильного назначения лечения следует обращаться к Вашему лечащему врачу.
Лейкоз: причины появления, симптомы, диагностика и способы лечения.
Определение
Лейкозы – большая группа заболеваний кроветворной системы. Кроветворение (гемопоэз) – это многоэтапный процесс образования форменных элементов крови в специализированных органах кроветворения. К форменным элементам крови относятся лейкоциты (белые кровяные тельца), которые участвуют во врожденном и приобретенном иммунитете, эритроциты (красные кровяные тельца), которые осуществляют транспорт кислорода и углекислого газа, и тромбоциты, обеспечивающие свертываемость крови.
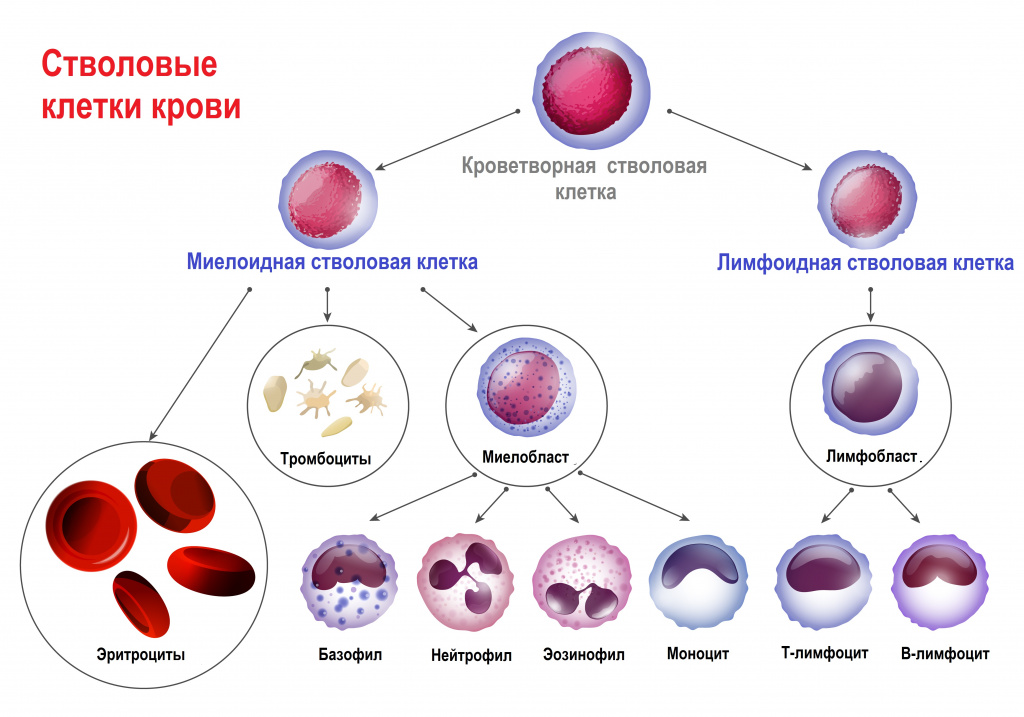
У всех клеток крови есть одна общая «родоначальница» – полипотентная стволовая клетка. Термин «полипотентная» означает, что такая клетка может развиваться в различные виды зрелых клеток.
Главный орган, где располагаются полипотентные стволовые клетки, – костный мозг, который как раз и поражается при лейкозах.
В результате повреждения (мутации) в генетическом материале полипотентной стволовой клетки-предшественницы нарушается процесс созревания клеток. При остром лейкозе возникает большое количество незрелых (бластных) клеток, из которых образуется опухоль, разрастается в костном мозге, замещает нормальные ростки кроветворения и имеет тенденцию к метастазированию – распространению с током крови или лимфы в здоровые органы. При хронических лейкозах заболевание течет годами, происходит частичная задержка созревания клеток и опухоль образуется из созревающих и зрелых клеток.
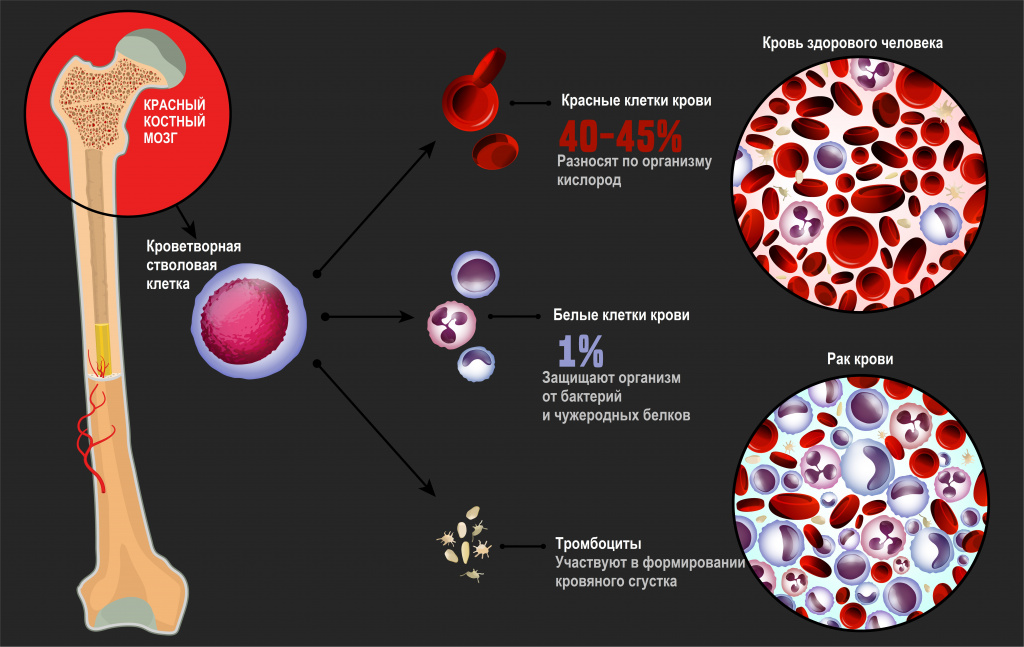
Причины возникновения лейкозов
К факторам риска развития лейкоза относятся:
- ионизирующая радиация: лучевая терапия по поводу других опухолей, облучение на рабочем месте, ультрафиолетовое излучение;
- воздействие на организм химических канцерогенных веществ;
- некоторые вирусы: HTLV (Т-лимфотропный вирус человека);
- бытовые факторы: добавки в пищевые продукты, курение, плохая экологическая обстановка;
- наследственная предрасположенность к раковым заболеваниям.
Лейкозы подразделяют на острые и хронические, а по типу поражения ростка кроветворения – на лимфоидные и миелоидные. Острый лейкоз никогда не переходит в хронический, а хронический не может стать острым (но его развитие может перейти в стадию бластного криза).
В зависимости от преобладания тех или иных опухолевых клеток выделяют бластные, цитарные и недифференцированные лейкозы.
Острый лимфобластный лейкоз (ОЛЛ) диагностируется у лиц любого возраста, начиная с младенческого и заканчивая пожилым, однако пик заболеваемости приходятся на детский возраст (60% пациентов с ОЛЛ моложе 20 лет). Острый лимфобластный лейкоз – самая распространенная опухоль кроветворной ткани у детей, которая составляет 30% всех злокачественных опухолей детского возраста. Заболеваемость ОЛЛ у пациентов пожилого возраста неуклонно возрастает: так, ежегодная частота ОЛЛ увеличивается с 0,39 случая на 100 тыс. населения в возрасте 35–39 лет, до 2,1 случая на 100 тыс. населения в возрасте ≥85 лет. Кроме того, приблизительно 30% ОЛЛ диагностируются в возрасте ≥60 лет.
Острым миелоидным лейкозом (ОМЛ) страдает в среднем 3-5 человек на 100 тыс. населения в год. Заболеваемость резко возрастает в возрасте старше 60 лет и составляет 12–13 случаев на 100 тыс. населения у лиц в возрасте старше 80 лет.
Хронический лимфобластный лейкоз (ХЛЛ) – самый частый вид лейкозов у взрослых, в то время как у детей этот вид опухоли не регистрируется. В европейских странах его частота составляет 4 случая на 100 тыс. населения в год и непосредственно связана с возрастом. У лиц старше 80 лет она составляет более 30 случаев на 100 тыс. в год.
Хронический миелолейкоз (ХМЛ) – редкое заболевание: 0,7 на 100 тыс. взрослого населения, пик заболеваемости приходится на 50-59 лет, однако до 33% больных ОМЛ – люди моложе 40 лет.
Симптомы лейкозов
Острый лейкоз в большинстве случаев дебютирует резко – внезапно повышается температура, появляются озноб, боль в горле, в суставах, отмечается резко выраженная слабость. Реже острый лейкоз может проявиться кровотечением. Иногда острый лейкоз начинается с постепенного ухудшения состояния больного, появления невыраженной боли в суставах и костях, кровоточивости. В единичных случаях возможно бессимптомное начало заболевания. У многих больных увеличиваются лимфоузлы и селезенка.
При хроническом лейкозе на начальной стадии, которая длится от года до трех лет, пациенты могут ни на что не жаловаться. Иногда беспокоят слабость, потливость, частые простудные заболевания, могут отмечаться тупые, ноющие боли в костях.
При подавлении эритроидного ростка, дающего красные кровяные тельца, возникает анемия и гемическая гипоксия (снижение количества кислорода в крови). При этом пациенты отмечают слабость, утомляемость, бледность кожных покровов.
При поражении мегакариоцитарного ростка падает количество тромбоцитов, поэтому возникает кровоточивость десен, слизистой оболочки носа, пищеварительного тракта, образуются синяки, кровоизлияния в различные органы. При прогрессировании лейкоза могут развиваться массивные кровотечения в результате ДВС синдрома (синдрома диссеминированного внутрисосудистого свертывания).
В результате недостатка лейкоцитов и снижения иммунитета развиваются инфекционные осложнения различной степени тяжести, что чаще всего проявляется лихорадкой.
Могут возникать язвенно-некротическая ангина, перитонзиллярные абсцессы, некротический гингивит, стоматит, пиодермия, параректальные абсцессы, пневмония, пиелонефрит. Существует значимый риск тяжелого течения инфекционных осложнений вплоть до развития сепсиса.
С током крови и лимфы опухолевые клетки попадают в здоровые органы, нарушают их структуру и функцию – наиболее подвержены метастатическим процессам печень, селезенка, лимфатические узлы, но метастазы могут поражать и кожу, и мозговые оболочки, и почки, и легкие.
Основные причины летальности у пациентов с лейкозом связаны с тем, что осложнения могут спровоцировать развитие сепсиса, полиорганную недостаточность, кровоизлияния в различные органы. Острый лейкоз без лечения приводит к смертельному исходу в течение нескольких недель или месяцев.
Диагностика лейкозов
Диагностика лейкозов основывается на оценке морфологических особенностей клеток костного мозга и периферической крови. Поэтому всем пациентам с подозрением на лейкоз назначают общий анализ крови с подсчетом лейкоцитарной формулы и определением числа тромбоцитов.
Клинический анализ крови – одно из основных лабораторных исследований для количественной и качественной оценки всех классов форменных элементов крови. Включает цитологическое исследование мазка крови с подсчетом процентного содержания разновидностей лейкоцитов (определение общего количества лейкоцитов и процентного соотношения основных субпопуляций лейкоцитов: нейтрофилов, лимфоцитов, моноцитов, эозинофилов и базофилов) и определение скорости оседания эритроцитов.
Для определения объема опухолевого поражения, вероятности развития синдрома лизиса опухоли рекомендовано выполнение общетерапевтического биохимического анализа крови: АСТ, АЛТ, общий билирубин, глюкоза, мочевина, креатинин, общий белок, ЛДГ, магний, натрий, калий, кальций.
Определение уровня АЛТ в сыворотке крови применяют преимущественно в диагностике и контроле течения болезней печени, а также в комплексных биохимических исследованиях.
Определение уровня АСТ в сыворотке крови используют преимущественно в диагностике и контроле течения болезней печени, а также в комплексных биохимических исследованиях.
Определение уровня билирубина в сыворотке крови используют для выявления поражений печени различного происхождения, закупорки желчных путей, гемолитической анемии, желтухи новорожденных.
Глюкоза – основной источник энергии для метаболических процессов в организме человека, является обязательным компонентом большинства внутриклеточных структур, участвует в синтезе нуклеиновых кислот (рибоза, дезоксирибоза), образует соединения с белками (гликопротеиды, протеогликаны) и липидами (гликолипиды).
Мочевина – конечный продукт расщепления белковых молекул, выводимый из организма почками. Определение уровня мочевины в сыворотке крови используют для оценки выделительной функции почек и контроля эффективности лечения пациентов с почечными заболеваниями.
Креатинин – продукт метаболизма мышечных клеток, удаляется из крови почками. Тест используют в качестве маркера функции почек для диагностики и мониторинга острых и хронических болезней почек, а также в скрининговых обследованиях.
Общий белок выступает показателем белкового обмена, отражающим содержание всех фракций белков в сыворотке крови. Тест используется в комплексных биохимических обследованиях пациентов при различных заболеваниях.
Лактатдегидрогеназа – гликолитический фермент, участвующий в конечных этапах превращений глюкозы. Тест используют в диагностике различных заболеваний (сердца, печени, мышц, почек, легких, системы крови).
Магний – один из основных катионов организма. Исследование магния в сыворотке крови в комплексе с другими электролитами используют для выявления нарушений электролитного баланса.
Определение уровня калия, натрия и хлора в сыворотке крови используется для скрининга электролитов и исследования кислотно-щелочного дисбаланса.
Общий кальций – основной компонент костной ткани и важнейший биогенный элемент, обладающий важными структурными, метаболическими и регуляторными функциями в организме.
Для определения вероятности развития тяжелых коагуляционных нарушений (как геморрагических, так и тромботических) рекомендовано исследование свертывающей системы крови.
Базовый набор тестов, применяемый для скрининговой оценки состояния свертывающей системы крови.
С целью исключения поражения почек выполняют общий анализ мочи.
Общий анализ мочи – комплексная оценка ряда физических и химических параметров мочи, а также элементов мочевого осадка, нацеленное на выявление патологии почек и мочевыводящих путей.
Диагностику хронического лейкоза проводят с помощью иммунофенотипического исследования лимфоцитов крови (ИФТ) методом проточной цитометрии.
Рекомендовано проведение стернальной пункции (пункции грудины) для получения цитологического препарата костного мозга и цитологическое и цитохимическое исследование мазка с целью уточнения диагноза и определения прогноза.
В ряде случаев показана биопсия опухолевого образования или лимфатического узла (или другого метастатического очага) и патологоанатомическое исследование полученного биопсийного материала.
Кроме того, врач может рекомендовать проведение иммунофенотипирования гемопоэтических клеток-предшественниц в костном мозге, цитогенетическое исследование аспирата костного мозга, молекулярно-генетические исследования мутаций в генах и др.
Из инструментальных методов диагностики проводятся:
-
эхокардиография для оценки функционального состояния сердечной мышцы;
Сканирование головного мозга, черепа и окружающих их тканей, позволяющее диагностировать различные патологии.
Исследование, позволяющее получить данные о состоянии органов грудной клетки и средостения.
Сканирование внутренних органов брюшной полости для оценки его функционального состояния и наличия патологии.
Лечение лейкозов
Лечение лейкозов проводится в стационаре. Медикаментозное воздействие на опухоль специальными препаратами, губительно действующими на быстро делящиеся клетки, называется химиотерапией. При лечении острых лейкозов химиотерапию проводят в несколько этапов: индукция ремиссии, консолидация (закрепление) ремиссии, поддерживающая терапия и профилактика нейролейкемии (метастазирования опухолевых лейкозных клеток в головной и спинной мозг).
Период индукции ремиссии – это начальный этап, цель которого максимально уменьшить опухолевую массу и достичь ремиссии. Обычно для этого требуется 1-2 курса химиотерапии. Далее идет консолидация достигнутого эффекта – наиболее агрессивный и высокодозный этап лечения, задачей которого является по возможности еще большее уменьшение числа остающихся после индукции лейкемических клеток. Этот этап также занимает 1-2 курса. За ним следует противорецидивное или поддерживающее лечение. При некоторых вариантах острых лейкозов требуется профилактика или, при необходимости, лечение нейролейкемии.
Для разных видов лейкозов у разных возрастных групп профессиональными сообществами разработаны схемы химиотерапии.
При лечении ХМЛ основными препаратами выбора являются ингибиторы тирозинкиназы, применяемые в непрерывном режиме – ежедневно, длительно, постоянно. Перерывы в приеме могут способствовать снижению эффективности терапии и прогрессированию заболевания. В случае неэффективности терапии может быть проведена трансплантацию гемопоэтических стволовых клеток или костного мозга.
В терапии ХЛЛ цели и схемы терапии химиотерапии определены возрастом пациента, числом и тяжестью сопутствующих заболеваний. Разработаны протоколы лечения для разных пациентов, в том числе схемы моно- и полихимиотерапии. Для профилактики инфекционных осложнений применяют внутривенное введение иммуноглобулина, рекомендована вакцинация от гриппа и пневмококковой инфекции.
Помимо химиотерапии пациенту может потребоваться трансфузионная терапия: переливание эритроцитарной массы, тромбоцитарной массы, изотонических растворов.
При присоединении инфекций показана антибиотикотерапия. На фоне лечения могут возникать тромботические осложнения, что требует антикоагулянтной терапии. Пациентам высокого риска в связи с вероятностью рецидива лейкоза применяют трансплантацию гемопоэтических стволовых клеток.
Осложнения
Основные осложнения лейкозов – инфекционные, вплоть до сепсиса, и тромботические и/или геморрагические осложнения с развитием синдрома диссеминированного внутрисосудистого свертывания. При метастазировании опухолевых клеток развивается полиорганная недостаточность, в т.ч. лейкозные клетки могут попадать в оболочки головного и спинного мозга, инфильтрировать периферические нервы с развитием разнообразных двигательных и чувствительных нарушений (лейкемоидная инфильтрация). Кроме того, встречается так называемый «синдром лизиса опухоли» – сложный процесс, возникающий в результате спонтанного или вызванного лечением разрушения большого числа опухолевых клеток с выходом внутриклеточного содержимого в кровоток. При этом может развиться острая почечная недостаточность. Летальность при лизисе опухоли достигает 70%.
Профилактика лейкозов
Так как причины возникновения лейкозов не установлены, методов специфической профилактики до сих пор не существует.
Однако доказано, что между курением и риском развития острого лейкоза существует дозовая зависимость, которая особенно очевидна для лиц старше 60 лет.
Ряд исследователей предполагают, что около 20% случаев ОМЛ являются следствием курения.
- Клинические рекомендации «Острые миелоидные лейкозы». Общероссийский национальный союз «Ассоциация онкологов России», некоммерческое партнерство содействия развитию гематологии и трансплантологии костного мозга «Национальное гематологическое общество», 2020.
- Клинические рекомендации «Острые лимфобластные лейкозы». Общероссийский национальный союз «Ассоциация онкологов России», некоммерческое партнерство содействия развитию гематологии и трансплантологии костного мозга «Национальное гематологическое общество», 2020.
- Клинические рекомендации «Хронический лимфоцитарный лейкоз/ лимфома из малых лимфоцитов». Общероссийский национальный союз «Ассоциация онкологов России», некоммерческое партнерство содействия развитию гематологии и трансплантологии костного мозга «Национальное гематологическое общество», региональная общественная организация «Общество онкогематологов», 2020.
- Клинические рекомендации «Хронический миелолейкоз у взрослых». Национальное гематологическое общество, 2017.
ВАЖНО!
Информацию из данного раздела нельзя использовать для самодиагностики и самолечения. В случае боли или иного обострения заболевания диагностические исследования должен назначать только лечащий врач. Для постановки диагноза и правильного назначения лечения следует обращаться к Вашему лечащему врачу.
Острый миелоидный лейкоз
Острый миелоидный лейкоз – это поражение костного мозга, из-за которого измененные белые кровяные клетки размножаются слишком быстро.
Заболевание, которое обыватели называют «раком крови», может возникнуть у людей любого пола и возраста, но чаще всего встречается у мужчин от 65 лет и старше.
Как развивается острый миелоидный лейкоз?
Острый миелоидный лейкоз (ОМЛ) начинается в костном мозге – мягкой внутренней части костей, состоящей из жировых и кроветворных клеток, включая стволовые, которые становятся:
- лимфоцитами, основной задачей которых является борьба с инфекциями и повреждением тканей;
- либо миелоидными клетками, способными превращаться в: белые и красные кровяные тельца, переносящие кислород из легких в другие ткани, а также тромбоциты, необходимые для остановки кровотечений – они помогают закрывать отверстия в сосудах, возникающие при порезах или ушибах.
Лейкоз начинается с изменения ДНК – содержащейся в каждой клетке нашего тела молекулы, в которой зашифрована вся информация об организме. Такие «поломки» возникают из-за воздействия химикатов, радиации, различных заболеваний или случайных сбоев, и приводят к производству слишком большого количества бластов – быстро растущих незрелых, то есть не работающих белых кровяных телец.
Нормальные бласты со временем превращаются в полезные клетки крови, а при лейкозе они становятся опухолевыми, активно размножаются и постепенно вытесняют нормальные, что приводит к ряду тяжелых последствий. У здорового человека их не много – они составляют 5% или меньше от костного мозга, а в крови не обнаруживаются. Для того, чтобы врач поставил диагноз «острый миелоидный лейкоз», их должно быть не менее 20%.
Такие клетки не просто циркулируют по организму – они распространяются в различные органы, включая лимфатические узлы, печень, селезенку, яички, головной и спинной мозг, скапливаются и повреждают их.
Врачи выделяют две основных формы миелоидного лейкоза:
– острый – развивающийся внезапно и быстро;
– и хронический – при данном типе заболевания бласты вытесняют здоровые клетки крови гораздо медленнее, чем при остром.
Причины возникновения острого миелоидного лейкоза
Точные причины развития данного заболевания врачам до сих пор не известны – они знают лишь о факторах, которые могут спровоцировать его возникновение:
- Возраст: острый миелоидный лейкоз возникает и у детей, и у взрослых, но чаще всего он обнаруживается у пожилых людей, а средний возраст постановки диагноза составляет около 68 лет.
- Курение – единственный доказанный фактор риска, связанный с образом жизни. Вредная привычка способна вызвать не только рак легких, рта или горла, поскольку ядовитый дым влияет и на клетки, которые не вступают с ним в прямой контакт. Содержащиеся в нем вещества поглощаются дыхательными путями и с кровью распространяются в различные части тела, в том числе в костный мозг.
- Химикаты: с развитием лейкоза связывают длительное воздействие бензола – растворителя, который используется в резиновой и автомобильной промышленности, а также на нефтеперерабатывающих заводах. Он содержится в бензине, сигаретном дыме, выхлопных газах машин, некоторых клеях, чистящих средствах и красках.
- Радиация: ее воздействие, в том числе полученное при лучевой терапии рака, увеличивает вероятность возникновения ОМЛ.
- Заболевания крови также относят к факторам риска, способным спровоцировать острый миелоидный лейкоз.
- Пол: взрослым мужчинам данный диагноз ставится чаще, чем женщинам, при этом среди юных пациентов мальчиков примерно столько же, сколько девочек. Причины такой статистики ученым до сих пор не известны.
- Генетические нарушения. Шанс образования ОМЛ повышен у обладателей различных генетических нарушений и особенностей, включая синдром Дауна Синдром Дауна – это генетическое нарушение, вызывающее умственную отсталость, задержку развития, пороки сердца и множество других проблем со здоровьем. У людей с данной особенностью развития есть не 46 хромосом, а на одну больше – 47. и трисомию 8 Трисомия 8 – это генетическое нарушение развития, у обладателей которого есть не две копии восьмой хромосомы, а целых три. .
- Лечение: заболевание чаще развивается у онкологических пациентов, которые получают определенные химиотерапевтические препараты. К ним относятся циклофосфамид, мехлорэтамин, прокарбазин, хлорамбуцил, мелфалан, бусульфан, кармустин, цисплатин, карбоплатин, этопозид, тенипозид, митоксантрон, эпирубицин и доксорубицин.
- Семейный анамнез: наличие близкого родственника – родителя, брата, сестры или детей – с данным диагнозом увеличивает риск развития данного заболевания.
Симптомы острого миелоидного лейкоза
Признаки лейкоза проявляются примерно одинаково как у детей, так и у взрослых, и могут выглядеть следующим образом:
- Обычно одними из первых симптомов становятся чрезмерная утомляемость и слабость. Они возникают из-за анемии – снижения количества красных кровяных телец, переносящих кислород ко всем тканям организма.
- Головокружения – еще один частый спутник заболевания. Самая вероятная причина их появления – все та же анемия, из-за которой мозгу не хватает О2.
- Внезапное снижение веса: как правило, люди худеют уже на ранних стадиях заболевания, в том числе из-за уменьшившегося аппетита.
- Синяки или кровоизлияния: по мере развития острого миелоидного лейкоза костный мозг производит все меньше тромбоцитов – клеток, отвечающих за свертывание крови. Когда их становится слишком мало, у человека легко появляются синяки и красные или фиолетовые пятна на коже, кровь идет из носа и десен, ее следы обнаруживаются в моче или стуле, а менструации становятся более обильными.
- Повышенная температура в любое время суток и ночная потливость: часто бывают вызваны в том числе инфекциями, развивающимися при нарушении работы кроветворной системы.
- Бледная или холодная кожа, а также чувствительность к низким температурам, вызванные анемией.
- Кровоточивость, боль и отеки десен: может быть признаком тромбоцитопении – нехватки необходимых для правильной свертываемости крови тромбоцитов.
- Одышка – ощущение нехватки воздуха: на ранних этапах лейкоза она обычно спровоцирована нехваткой переносящих кислород клеток, а на поздних может быть вызвана тромбоэмболией – закупоркой легочной артерии. Это серьезное осложнение вызывает целый комплекс симптомов, таких как боль в груди, шее, плечах, руках и челюсти, тревожность и беспокойство, аритмия – неправильный ритм сердцебиения, тахикардия – слишком частое сокращение сердца, и обмороки.
- Частые инфекции – еще один признак заболевания, который появляется из-за присутствия в организме большого количества измененных белых кровяных телец. Их избыток приводит к нехватке нормальных нейтрофилов – клеток, которые борются с бактериями и грибками.
- Лейкостаз: скопление измененных клеток в сосудах, что приводит к появлению похожих на инсульт Инсульт – это нарушение кровообращения в головном мозге. симптомов: сонливости, головным болям, онемению лица, нехватке воздуха, нарушениям зрения, слабости и даже проблемам с речью.
- Вздутие живота: не самая распространенная проблема у обладателей острого миелоидного лейкоза. Она возникает при накоплении неправильных клеток в селезенке и печени, что приводит к нарушению пищеварения.
- Сыпь или уплотнения: наблюдаются примерно у 10% пациентов. Их наличие может говорить о распространении болезни на кожу.
- Еще один возможный симптом – боль в суставах и костях из-за присутствия в них большого количества измененных клеток.
- Головные боли – могут быть признаком как анемии, так и повреждения мозга.
- Увеличение лимфатических узлов – наших крошечных «фильтров», задерживающих и обезвреживающих опасные вещества. Часто они ощущаются как небольшие образования размером с горошину – под кожей в области шеи, подмышек или паха.
Диагностика острого миелоидного лейкоза
Тщательная диагностика крайне важна, поскольку в ее ходе доктор может не только установить сам факт наличия заболевания, но и понять, какое именно лечение подходит конкретному пациенту.
Диагностика начинается с обычного медицинского осмотра и поисков синяков, кровоподтеков или возможных признаков инфекции, после чего назначается целый ряд процедур:
- Анализы крови: позволяют видеть ее состав, обнаруживать измененные клетки, а также оценивать работу внутренних органов, таких как печень или почки.
- Сбор образцов костного мозга: процедура обязательная, поскольку именно в нем начинает развиваться заболевание. Как правило, пробы забирают из задней части тазовой или грудной костей в ходе двух болезненных, одновременно проводимых процедур. При аспирации пациент ложится на бок или живот, врач очищает кожу бедра, обезболивает ткани и вводит в них тонкую иглу, после чего шприцем отсасывает небольшое количество жидкого костного мозга. При биопсии специалист с помощью более толстой иглы удаляет еще и небольшие кусочки кости.
- Анализ спинномозговой жидкости – люмбальная, или спинномозговая пункция: назначается, если у человека есть симптомы, которые могут быть вызваны распространением измененных клеток в головной или спинной мозг. При сборе образцов доктор обезболивает участок кожи в нижней части спины над позвоночником, и вводит небольшую иглу в область между позвонками.
- Молекулярные и генетические тесты: необходимы для обнаружения мутаций, или изменений, в генах. Такие данные необходимы врачам для подбора оптимального лечения.
- Визуальные исследования – УЗИ, рентген, КТ, МРТ или ПЭТ: создают изображения внутренних тканей тела. Их назначают не для выявления лейкоза как такового, а для обнаружения инфекций, других проблем со здоровьем или определения запущенности заболевания, если специалисты считают, что оно распространилось за пределы костного мозга.
Лечение острого миелоидного лейкоза
Борьба с лейкозом – задача сложная и требует участия сразу нескольких врачей – не только гематолога, но и онколога, химиотерапевта и других.
В Онкоцентре «Лапино-2» есть целая команда отличных специалистов, которые не просто быстро выявят заболевание, но и проведут любые необходимые лечебные процедуры.
Вам не придется задаваться вопросом «что делать?» и «к кому обращаться?» – у нас вы получите четкий план действий, следуя которому пройдете терапию без очередей, задержек и нервов.

При лечении миелоидного лейкоза врачи применяют несколько методов.
-
Химиотерапия – уничтожение измененных клеток специальными препаратами. Такие вещества вводятся с помощью капельниц или принимаются в виде таблеток, попадают в кровь и распространяются по всему организму.
- Индукция ремиссии: первая фаза, задача которой заключается в быстром сокращении как можно большего количества лейкозных клеток. Во время ее проведения человек обычно находится в лечебном учреждении, поскольку лекарства разрушают не только неправильные, но и нормальные клетки костного мозга. В результате такого воздействия на организм показатели крови становятся опасно низкими, из-за чего самочувствие больного ухудшается. Многим людям приходится принимать антибиотики и препараты, повышающие количество белых кровяных телец, а некоторым требуется переливание крови. Примерно через неделю после окончания химиотерапии врач проводит биопсию и изучает состояние изъятых тканей. У большинства пациентов после первого же курса наступает ремиссия – бласты Бласты – это быстро растущие незрелые, не работающие белые кровяные тельца. составляют не более 5% от общего объема костного мозга. Если анализы выявляют их избыток, человеку назначают повторное лечение, либо рекомендуют пересадку стволовых клеток Стволовые клетки, производимые костным мозгом, могут становиться: красными кровяными тельцами, переносящими кислород по телу; лейкоцитами, помогающими бороться с инфекциями; и тромбоцитами, которые останавливают кровотечения.) . Во время этапа индукции все бласты обычно убить не получается – небольшая их часть все же остается в организме. В таком случае терапию нужно продолжить, поскольку иначе заболевание может вернуться в течение нескольких месяцев.
- Консолидация – вторая фаза, назначаемая для полного уничтожения измененных клеток и предотвращения рецидива – повторного развития лейкоза. Ее схема подбирается индивидуально для каждого пациента – она зависит не только от общего состояния здоровья человека, но и от его возраста.
- аллогенную трансплантацию клеток подходящего донора – близкого родственника, такого как брат или сестра, или другого добровольца;
- или пересадку аутологичных – собственных стволовых клеток человека, изъятых и замороженных еще до начала курса «химии».
- одни блокируют белки, которые помогают неправильным клеткам расти;
- вторые помогают им превращаться в нормальные;
- третьи убивают их при попытке разделения для создания новых;
- четвертые нацелены на белки, помогающие им жить слишком долго;
- пятые снижают выживаемость и уменьшают рост лейкозных клеток.
- при распространении заболевания за пределы костного мозга и крови: например, в мозг, спинномозговую жидкость или яички;
- перед трансплантацией стволовых клеток Стволовые клетки, производимые костным мозгом, могут становиться: красными кровяными тельцами, переносящими кислород по телу; лейкоцитами, помогающими бороться с инфекциями; и тромбоцитами, которые останавливают кровотечения.) ;
- для сокращения опухолей, которые давят на трахею – дыхательное горло, и не позволяют человеку получать достаточное количество кислорода;
- для уменьшения боли в области пораженной кости, если этого не удалось добиться с помощью химиотерапии.
Статус острого миелоидного лейкоза после лечения
Долгосрочные прогнозы каждого пациента в немалой степени зависят от того, насколько хорошо и быстро заболевание поддается лечению: чем лучше первая реакция организма, тем оптимистичнее перспективы.
Ремиссия – отсутствие признаков лейкоза: в костном мозге содержится меньше 5% бластов Бласты – это быстро растущие незрелые, не работающие белые кровяные тельца. , а количество клеток крови находится в пределах нормы. Полная молекулярная ремиссия означает, что врачам не удалось обнаружить измененные клетки даже с помощью очень чувствительных тестов.
Минимальная остаточная болезнь , МОБ: данный термин используется в тех случаях, когда после проведения терапии неправильные клетки не обнаруживаются обычными методами – например, при стандартном осмотре образцов под микроскопом, но выявляются при проведении современных точных исследований.
Активное заболевание: после лечения в костном мозге есть больше 5% бластов, либо после проведенной терапии произошел рецидив – возвращение болезни.

Прогнозы и выживаемость при остром миелоидном лейкозе
Перспективы каждого человека индивидуальны и зависят от большого количества факторов.
Немаловажную роль играет возраст – например, люди старше 60 обычно уже имеют хронические проблемы со здоровьем, которые усугубляют ситуацию. Кроме того, их организм тяжело переносит сильнодействующие химиотерапевтические препараты и другие виды лечения. По данным исследований , только 40% пациентов в возрасте от 65 лет способны получать подобные вещества на протяжении 3 месяцев.
Для каждого вида заболевания есть своя статистика.
После индукции – первого же курса химиотерапии выходят в ремиссию, то есть нормализуют количество клеток крови, около 90% обладателей острого промиелоцитарного лейкоза. Для всех остальных типов эта цифра составляет примерно 67%.
Кроме того, многие люди 60+ не реагируют на лечение, и всего лишь у половины из них после индукции наступает ремиссия.
Пятилетняя выживаемость – вероятность прожить 5 или больше лет с даты постановки диагноза, для взрослых составляет около 27,4% . Это означает, что спустя 5 лет с момента обнаружения заболевания в живых остается 27,4% пациентов.
У детей статистика своя: от 85% до 90% из них выходят в ремиссию после индукции, а их пятилетняя выживаемость составляет от 60% до 70%.
Лейкоз — симптомы, лечение острого и хронического лейкоза у детей и взрослых
Лейкоз — это опухолевое поражение кроветворной системы. Первично опухоль поражает костный мозг и вызывает нарушение функций и уменьшение количества белых клеток крови, которые защищают организм от чужеродных патогенных микроорганизмов. Лейкоз может быть острым и хроническим. Его чаще выявляют у детей, но это заболевание поражает и взрослых.

Отличия острого и хронического лейкоза
Лейкоз также называют лейкемией или гемобластозом. Это онкологическое заболевание, для которого характерны мутации клеток костного мозга, которые в результате перерождаются в раковые. Они присутствуют в костном мозге — основном кроветворном органе, а также в крови, лимфатических узлах.
Различают острую и хроническую лейкемию. Отличие первой состоит в том, что ее основная масса представлена молодыми клетками. При хроническом лейкозе она состоит из зрелых и созревающих клеток. Острый лейкоз прогрессирует очень быстро, хронический склонен к медленному развитию.
Лейкоз бывает миелобластным и лимфобластным. Названия даны в соответствии с предшественниками клеток — миелобластами и лимфобластами.
При остром и хроническом лейкозе в крови появляются бластные формы клеток, то есть незрелые, которые при нормальных условиях созревают и превращаются в функциональные клетки крови.
Острые лейкозы чаще выявляют у детей, хронические — у взрослых.
Причины
Как и в отношении других видов рака, точная причина развития лейкоза не установлена. Предположительно, его могут провоцировать:
- генетические мутации;
- действие радиации;
- наследственный фактор;
- воздействие канцерогенов;
- хромосомные аномалии (болезнь Дауна, синдром Вискотта-Олдрича);
- перенесенная ранее химиотерапия по поводу другого вида рака;
- сопутствующие заболевания крови (отдельные формы анемии, миелодисплазии).
С возрастом риск развития лейкоза повышается.
Перечисленные причины можно назвать условными: часто у пациентов нет ни одного из факторов риска, и, наоборот, многие люди из группы риска никогда не заболевают раком крови.
Симптомы
Проявления лейкоза часто обнаруживаются на запущенной стадии. Хроническая форма заболевания может долго, в течение нескольких месяцев и даже лет, протекать бессимптомно.
Острый лейкоз проявляется в:
- умеренной слабости и утомляемости на начальной стадии;
- бледности кожных покровов;
- беспричинном повышении температуры до 37-37,5 градусов;
- кровоточивости десен;
- обильных менструациях у женщин;
- увеличении лимфоузлов;
- продолжительной кровоточивости ран;
- кровоизлияниях в кожу;
- выраженных суставных болях;
- повышенной потливости.
Из-за снижения уровня лейкоцитов организм становится более восприимчивым к инфекциям, поэтому они часто повторяются.
В запущенных случаях возникает выраженная болезненность костей.
Для хронического лейкоза характерны аналогичные симптомы, но они смазаны и развиваются в течение долгого времени.
Диагностика
Для постановки диагноза «лейкемия» проводят следующие процедуры:
- развернутый анализ крови;
- коагулограмма;
- пункция костного мозга;
- рентгенография черепа и органов грудной клетки;
- УЗИ лимфатических узлов, селезенки и печени;
- электрокардиография.

Дифференциальная диагностика лейкоза направлена на исключение инфекционного мононуклеоза, ВИЧ-инфекции, фолиеводефицитной анемии, тромбоцитопенической пурпуры.
Лечение лейкоза у детей и взрослых
При остром и хроническом лейкозе основой лечения выступает химиотерапия. Для борьбы с заболеванием используют сильные лекарственные средства, которые содержат вещества, направленные против роста опухолевых клеток. Препараты останавливают их рост, замедляют деление либо в целом уничтожают.
Препараты разного типа предназначены для разного применения:
- перорального;
- внутривенного;
- интратекального (введение средства в спинномозговую жидкость).
Выбор конкретного препарата зависит от общего состояния пациента.
Химиотерапия включает несколько фаз. Это:
- Индукция. На этом этапе происходит уничтожение бластных клеток в крови и костном мозге. Благодаря этому удается достичь ремиссии.
- Консолидация (интенсификация). Цель терапии на данном этапе — уничтожение всех оставшихся раковых клеток, способных спровоцировать повторное развитие лейкоза (рецидив).
- Стабилизация. Это поддерживающая терапия, направленная на подавление опухолевых клеток, которые могли остаться в организме после пройденных ранее этапов химиотерапии. Фаза стабилизации может продолжаться несколько лет.
Пациентам, у которых наблюдается устойчивая к химиотерапии форма рака, назначают трансплантацию костного мозга. Этот метод также остается единственным эффективным у лиц с высоким риском рецидива.
Пациентам с лейкемией требуется костный мозг от генетически совместимого или частично совместимого донора. Им может быть как родственник, так и любой совместимый человек, не являющийся родственником пациента.
Поиск неродственного донора осуществляется в регистре доноров костного мозга.
Реабилитация после лечения
Химиотерапия оказывает мощное воздействие на организм, причем не только на опухолевые, но и на здоровые клетки. После лечения пациентам требуется профессиональная реабилитация, направленная на устранение последствий и осложнений лечения лейкоза. К ним относятся:
- тошнота и рвота;
- анемия;
- снижение аппетита;
- стоматит;
- нарушение микрофлоры кишечника;
- диарея или запоры;
- сухость и зуд кожи;
- повышение температуры;
- болевой синдром;
- чувство жжения, онемения, холода без воздействия внешних факторов.

Для пациентов, которые прошли химиотерапию и другие виды лечения лейкемии, подбирают восстановительные программы в зависимости от преобладающих симптомов.
Отдаленные последствия лейкозов
Лейкемия может вызывать проблемы со здоровьем даже спустя месяцы и годы после диагностирования заболевания или завершения лечения. Именно поэтому тем, кто перенес это заболевание, необходимо регулярно наблюдаться у специалиста.
К отдаленным последствиям лейкозов относят:
- рецидив заболевания;
- образование вторичных очагов лейкоза (метастазов) в мягких тканях, молочных железах, коже, головном мозге;
- нарушения функций сердца и легких;
- нарушения психики, логического мышления, способности к планированию;
- отклонения в работе эндокринной системы;
- депрессии.
При своевременно начатом лечении лейкемии, а также адекватной терапии, 80-90% больных достигают полной ремиссии. После трансплантации костного мозга вероятность долговременного выживания также довольно высокая: она составляет около 80%.
При отсутствии лечения лейкоз становится причиной смерти больного через 1-2 года после диагностирования заболевания в острой форме.


