Хронический хламидийный простатит: особенности терапии
У мужчин урогенитальный хламидиоз чаще всего бывает в форме уретрита, который в отличие от гонорейного протекает, как правило, подостро с небольшими выделениями и незначительными дизурическими расстройствами или торпидно, субманифестно, когда больные замечают только незначительные слизистые выделения из уретры по утрам или только склеивание наружного отверстия мочеиспускательного канала. Поэтому зачастую уретрит распознается врачом только тогда, когда больной обращается уже осложнением. Хламидийный уретрит очень часто протекает в виде смешанной инфекции с другими возбудителями ИППП: трихомонадами, гонококками, уреплазмами, гарднереллами, вирусом герпеса I и II иммунотипов.
Наиболее частым осложнением урогенитального хламидиоза является хронический простатит . У 75% мужчин, страдавших хроническим хламидийным уретритом, выявляется хронический простатит. Его частота в общей структуре простатита оценивается исследователями в 28–56%. Роль Chlamydia trachomatis в развитии хронического простатита подтверждает их наличие в секрете железы или ее тканях, полученных трансректальной или трансперинеальной пункцией железы, т.е. в условиях, исключающих контаминацию исследуемого материала хламидиями из уретры.
Хронический хламидийный простатит сопровождается симптомами, которые свойственны уретриту, – наличие парастезий и болей в области промежности, крестца и прямой кишки (ощущение тяжести, давления), усиливающихся при длительном сидении, дефекации, езде в транспорте и т. д., иногда иррадиирующих в половой член, мошонку, крестец, поясницу. Начинаются функциональные расстройства. Они складываются из расстройств:
· нервной системы и психики в форме вторичного неврастенического синдрома, бессонницы, повышенной утомляемости, снижения работоспособности;
Примерно у 2/3 больных хронический хламидийный простатит протекает бессимптомно. У остальных сопровождается обострениями. При определенных иммунопатогенетических особенностях организма (наличие антигена др.) хламидийный простатит приводит к развитию болезни Рейтера.
Сложности терапии хронического хламидийного простатита, практически в каждом случае ассоциирующегося с хламидийным воспалением уретры (обычно хроническим и сопровождающимся эндоуретральными осложнениями) обусловлены биологическими особенностями возбудителя – C.trachomatis. Располагаясь внутри клетки во включениях, окруженных наружной мембраной высоко инфекционные элементарные тельца хламидий недосягаемы для противохламидийных антибактериальных препаратов и не испытывают никаких агрессивных влияний со стороны антител или других защитных факторов организма. Даже те антибиотики (азитромицин и др.), которые проникают внутрь клетки, как правило, концентрируются в лизосомах. Они бездействуют за трехслойной мембраной лизосом, поскольку у хламидий есть уникальное свойство – блокировать механизм лизосомного слияния с мембраной включения, препятствуя, таким образом, и фагоцитарному килингу, и воздействию антибиотиков.
Элементарные тельца, попавшие в межклеточные пространства, не одновременно фагоцитируются чувствительными клетками. Поэтому, микроколонии хламидий в различных клетках находятся на разных стадиях развития. некоторые элементарные тельца могут определенное время сохраняться в межклеточных пространствах нефагоцитированными. Это чрезвычайно важно для понимания того, что у антибактериальной терапии урогенитальных хламидиозов и, в частности, хронического хламидийного простатита, возможности ограничены . Дело в том, что спороподобные метаболически малоактивные элементарные тельца, располагаясь в межклеточных пространствах, мало подвержены влиянию препаратов, способных разрушать микроколонии хламидий в клеточных культурах. Даже антисептики, используемые для профилактики классических венерических инфекций, недостаточно эффективны при хламидии. Так, оказалась бесполезной профилактика урогениталного хламидиоза 0,05% раствором хлоргексидина биглюконата (гебитана) и некоторыми другими небарьерными средствами, эффективными при сифилисе, гонорее, трихомониазе.
Чувствительными для антибактериальных препаратов являются только РТ в период активной жизни, но именно в это время они находятся за мембраной включений.
Важным фактором в патогенезе хламидийной инфекции принято считать ее персистенцию , т. е. постоянное нахождение хламидий внутри без роста и размножения. Особенно повышается резистентность хламидий к лечению больных хроническим хламидиозом, в частности, хроническим хламидийным простатитом. Это обусловлено особыми взаимоотношениями возбудителя с макроорганизмом в связи с неудачами предшествующего лечения, нарушением иммунного статуса и регуляторных факторов иммунной системы (снижение общего количества иммунорегуляторного индекса, и др.). Медиаторами персистенции хламидий могут быть пенициллин, хлортетрациклин, левомицетин, способные ингибировать внутриклеточный цикл развития хламидий. Временное краткосрочное подавление хламидийной инфекции может произойти неадекватных режимов антибиотикотерапии либо нерациональной дозы или длительности терапии. При персистирующей хламидийной инфекции хламидии не реагируют на антибиотик так, как нормальные, циклично развивающиеся формы возбудителя. Предполагается, что причина может заключаться в снижении количества основного белка оболочки (МОМР) хламидий, в отсутствии которого многие антибиотики не транспортируются внутрь хламидийной клетки.
Таким образом, антибактериальная терапия у больных урогенитальным хламидиозом нередко приводит не к ликвидации инфекционного агента, а лишь к стиханию клинических проявлений, к переводу манифестного процесса в малосимптомный, субклинический или латентный хламидиоз (бессимптомное носительство хламидий). Такие люди не считают себя больными и служат резервуаром хламидийной инфекции. Кроме того, у этих пациентов возбудители могут приобретать резистентность к тетрациклинам, рифампицину и другим препаратам.
Химиотерапия хронического хламидийного простатита осложняется, благодаря изменению рН предстательной железы в щелочную сторону, что существенно затрудняет диффузию противохламидийных препаратов в ткань железы. Усложняется лечение и при ассоциации хламидий с другими возбудителями ИППП или микрофлорой, персистирующей как в уретре, так и в предстательной железе.
Наш многолетний опыт позволяет утверждать, что одной этиотропной противохламидийной терапии явно недостаточно для этиологического и клинического излечения больных хроническим хламидийным простатитом. Мы применяем комплексную терапию, включающую методы стимуляции защитных реакций организма (пирогенал, иммуномодуляторы), протеолитические ферменты, противохламидийные антибиотики и тщательное местное лечение с использованием различных средств непосредственного воздействия на очаги воспаления в уретре и предстательной железе, в том числе и физиотерапию.
Противохламидийную антибиотикотерапию следует проводить в течение 3–4 недель ( табл.1 ).
Исходя из биологических особенностей хламидий, прежде всего, устойчивости элементарных телец к антибактериальным препаратам, мы считаем, что нельзя рассчитывать на успех кратковременных курсов лечения противохламидийными средствами. В то же время рациональным можно считать отказ от длительного непрерывного приема антибиотиков. В качестве альтернативы крупнейший российский венеролог И.И. Ильин предлагает применять при лечении хронического хламидийного простатита своеобразную По мнению автора, она необходима для того, чтобы оставшиеся после первого курса ударной химиотерапии интактные элементарные тельца в межклеточных пространствах были бы фагоцитированы во время перерыва в лечении чувствительными клетками и в них сформировались бы микроорганизмы, которые могут погибнуть от последующих курсов противохламидийных средств. Такой курс не должен превышать 7–10 дней, что соответствует 3–4 циклам формирования микроколоний из элементарных телец. Затем, после приблизительно такого же интервала, курс лечения необходимо повторить еще 2–3 раза. Например, в начале, в течение 10 дней назначались тетрациклины (доксициклин), затем перерыв на 5–7 дней, потом курс лечения азитромицином или ципролетом, вновь перерыв и опять курс лечения, но уже доксициклином. И.И. Ильин считает, что короткие курсы более физиологичны, чем длительный непрерывный прием антибиотиков, заметно угнетающий иммунную реактивность организма, способствующий развитию дисбактериоза, кандидоза и пр.
Острый и хронический хламидийный простатит
Острый хламидийный простатит возникает как следствие хламидиоза органов мочеполовой системы.
Хронический хламидийный простатит является следствием неправильного лечения острой формы этого заболевания.
Инфекционным агентом заболевания является хламидия – внутриклеточный паразит.

Заражение преимущественно происходит при незащищенном сексе.
При недостаточном иммунитете или неверно подобранной терапии возбудители болезни поражают предстательную железу.
Важно! Хронический хламидийный простатит и его острая форма составляют 30% от общего числа простатитов.
Лечение хламидийного простатита необходимо для сохранения здоровья мужчины.
Хламидийный простатит: симптомы
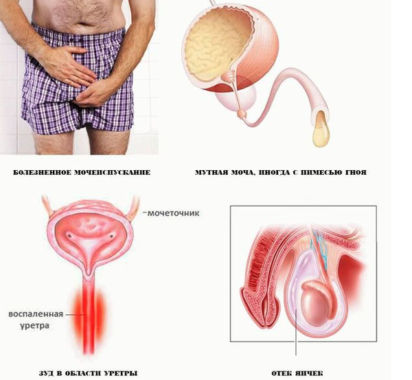
Выделяют следующие признаки хламидийного простатита.
- Тянущее чувство в прямой кишке.
- Болевые ощущения в области промежности.
- Патологические выделения из прямой кишки и мочеиспускательного канала.
- Часты позывы к мочеиспусканию, в том числе ложные.
- Зуд и жжение в мочеиспускательном канале.
- Повышение температуры тела.
- Нарушение эрекции.
- Выделение мутной мочи с примесями.
- Затруднения с достижением оргазма.
- Преждевременная эякуляция.
Симптомы могут сопровождаться чувством общей усталости и другими признаками интоксикации организма.
При пальпации или визуальном исследовании простаты отмечается ее увеличение или деформация.
Хронический хламидийный простатит характеризуется чередованием обострений и скрытых периодов болезни.
Возобновление симптомов при хронической форме заболевания происходит на фоне ослабления организма.
Обострение может быть вызвано болезнями, нервной перегрузкой, переохлаждением и другими стрессовыми факторами.

О симптомах и лечении острого
и хронического хламидийного
простатита
рассказывает подполковник
медицинской службы, врач
Ленкин Сергей Геннадьевич
Содержание данной статьи проверено и подтверждено на соответствие медицинским
стандартам врачем дерматовенерологом, урологом, к.м.н.
Ленкиным Сергеем Геннадьевичем
| Наименование | Срок | Цена |
|---|---|---|
| Прием уролога | 900.00 руб. | |
| ДНК Chlamydia trachomatis | 1 д. | 300.00 руб. |
| Массаж простаты | 600.00 руб. |
Лечение хламидийного простатита
Лечение хламидийного простатита осуществляет врач-уролог или дерматовенеролог.
Прежде, чем назначить лечение, врач уточняет причину заболевания при помощи дополнительных исследований.
Для подтверждения диагноза используются следующие методы.
- I. Бактериологический или ПЦР анализ мазка из уретры.
- II. Анализ спермы, на присутствие в ней хламидий.
- III. Анализ секрета предстательной железы.
- IV. УЗИ простаты и органов малого таза.
Основными препаратами, которыми осуществляется лечение хламидийного простатита, являются антибиотики.
Бактериологический анализ позволяет выявить наиболее эффективные антибактериальные препараты для данного штамма.
Антибиотики могут назначаться в виде таблеток или инъекций.
Эффективным методом лечения хламидийного простатита, особенно в хронической форме, считается лимфотропная терапия.
Этот метод основан на вводе лекарственных средств напрямую в воспаленную паренхиму простаты.
Эндолимфатический способ лечения тоже приветствуется.
Лекарства вводятся в лимфатический сосуд, что обеспечивает максимальное действие препарата.
Кроме уничтожения возбудителя, требуется общее укрепление организма.
Для этого используют иммуномодуляторы и витамины.
Лечение хламидийного простатита требует и физиотерапевтического лечения.
Основной процедурой является массаж простаты.
Этот метод предотвращает застой секрета и улучшает кровоснабжение предстательной железы.
Помимо этого, используется лазерная терапия и электростимуляция.
Для борьбы с нарушением кровообращения в области малого таза назначается курс физических упражнений.
Важно! Хронический хламидийный простатит без лечения может привести к мужскому бесплодию.
Для подбора оптимальной терапии хронического хламидийного простатита, обращайтесь к специалистам нашей клиники.
Хламидиоз-скрытая болезнь с опасными последствиям!
Хламидии — группа облигатных внутриклеточных паразитов, занимающих промежуточное положение между бактериями и вирусами.
Chlamydia trachomatis — основной возбудитель одного из самых распространненых заболеваний, передающихся половым путем — хламидиоза. Каждый год в мире хламидиозом заболевает около 90 млн человек. Хламидийной инфекцией страдает почти половина мужчин активного сексуального возраста (от 16 до 40 лет) и треть женщин. Хламидиями инфицированно 30-60% женщин и до 51% мужчин. Очень часто молодые пары, планирующие завести детей, сталкиваются с проблемой бесплодия одного из партнёров. Причиной этому может быть Хламидиоз. Как известно, одна из шести пар страдает от бесплодия, и примерно в половине случаев это проблема мужчины. В Европе около 600 000 случаев сальпингита оценены как следствие хламидийной инфекции, приводящей к проблеме бесплодия в четвёртой части из них.
Chlamydia trachomatis поражает в основном мочеполовую систему и наиболее часто проявляется у мужчин и женщин после инкубационного периода продолжительностью от 5 до 30 дней, при этом вызывая широкий спектр патологий. Широкое распространение хламидийной инфекции в первую очередь связано с бессимптомным течением заболевания.
Долгое время, скрытно существуя в организме пациента и никак себя не проявляя, хламидии, при неблагоприятных для них условиях (воздействие сильных антибиотиков, перегревание, переохлаждение, простуда, усиление иммунитета) способны трансформироваться в так называемые L-формы — как бы «впадая в спячку», при этом приобретая защитную оболочку позволяющую существовать во «враждебной» для них среде организма. Только в период иммуносупрессии (подавления защитных сил) возможно активное размножение и так называемая реверсия (пробуждение) хламидий из L-форм. Данный феномен способствует длительному внутриклеточному паразитированию без конфликтов с иммунной системой хозяина/
Заражение происходит половым путем. Передача хламидийной инфекции через загрязненные инфицированным отделяемым руки, белье и др. существенного эпидемиологического значения не имеет. Четко установлена высокая частота инфицирования хламидиями (более 50%) — новорожденных во время родов при прохождении их через инфицированные родовые пути, а также внутриутробная передача инфекции.
Течение мочеполового хламидиоза очень разнообразно и может принимать абсолютно разные формы. Наиболее коварным является бессимптомное течение инфекции.
У мужчин первично поражается мочеиспускательный канал, а затем и другие органы (предстательная железа, семенные пузырьки, придатки яичек). Среди возможных и опасных осложнений хламидиоза у мужчин — уретриты, хронический хламидийный простатит, кисты предстательной железы.
У женщин поражается канал шейки матки, после чего может возникнуть и восходящая инфекция, захватывающая матку, маточные трубы, яичники и брюшину. Хламидийная инфекция часто поражает шейку матки и мочеиспускательный канал одновременно. Хламидии из мочеиспускательного канала способны проникать в мочевой пузырь, вызывая цистоуретрит. Хламидии, локализующиеся в женских мочеполовых органах, предрасполагают к возникновению патологии беременности.
При обостренных формах заболевания наблюдается изменение слизистых оболочек мочеполовых органов, слизисто-гнойные неприятно пахнущие выделения из уретры, влагалища, частые позывы на мочеиспускание, неприятные ощущения в области таза, чувство распирания в промежности, зуд и сильные боли в мочеиспускательном канале.
Так же часто встречаются лица, у которых полностью отсутствуют клинические симптомы выделений из мочеполовых органов. Они не отмечают и не предъявляют жалоб на остальные симптомы. Хламидии у них выявляются только при клинических исследованиях, то есть имеют место случаи носительства хламидийной инфекции.
Хламидийная инфекция это очень опасный враг, способный нанести внезапный удар по самому ценному и дорогому в жизни любой семьи, лишить семью возможности иметь детей. Бесплодные браки – это очень частое явление во всём мире. Причиной бесплодия не редко становится хламидиоз. Перенесённый ранее в латентной форме или недолеченный хламидиоз, переходит в хроническую стадию. Хламидиоз часто сочетается с другими ИППП – гонореей, трихомониазом, гарднереллезом, уреаплазмозом, вирусами. В результате всего этого осложнения хламидиоза часто проявляются заболеваниями мочеполового тракта: уретрит, цистит, пиелонефрит, эпидидимит, орхит, простатит, эндометрит и др. Помимо многочисленных осложнений хламидиоза, касающихся половых органов, хламидийная инфекция может вызывать поражение других органов и систем. Болезнь Рейтера сопровождается поражением глаз (хламидийный конъюктивит), суставов (голеностопные, коленные, тазобедренные, позвоночник) с развитием реактивных артритов, уретрита хламидийной этиологии. Хламидиоз у женщин вызывает целый ряд осложнений, в том числе и бесплодие (непроходимость маточных труб). При восходящей хламидийной инфекции поражаются слизистая оболочка матки (эндометрий), трубы, яичники, связочный аппарат матки, брюшина, печень. наиболее часто хламидийной инфекцией поражаются трубы, причем заболевание носит подострое хроническое течение, вследствие чего развивается непроходимость маточных труб и бесплодие. Хламидийная инфекция может выявляться и у беременных женщин, причем заражение возможно во время беременности или диагностируется ранее, как правило это хронически протекающая инфекция. Наличие хламидийной инфекции у беременных женщин повышает риск угрозы невынашивания, самопроизвольного выкидыша, неразвивающейся беременности, мертворождения, преждевременных родов, несвоевременного излития околоплодных вод, осложнений в родах и послеродовом периоде, а также заражения плода при прохождении через родовые пути.
Совокупность всех современных диагностических методов дает возможность получить полную и наиболее достоверную картину заболевания. Диагноз хламидиоза ставится на основании истории болезни, оценки клинических признаков заболевания и лабораторных анализов. В связи с тем, что для генитального хламидиоза часто характерно малосимптомное течение, основное значение имеет лабораторная диагностика этой инфекции.
Лабораторная диагностика хламидийной инфекции
молекулярная диагностика методом ПЦР (ДНК Chlamydia trachomatis (сокоб))
иммуноферментный анализ (антитела IgG, IgМ, IgА к Chlamydia trachomatis).
Метод молекулярной диагностики является «золотым стандартом» диагностики хламидиоза во всем мире. Используемые в сочетании, оба анализа (ПЦР и иммуноферментный анализ) позволяют нивелировать некоторые недостатки друг друга при использовании их в отдельности (если хламидия не будет обнаружена в соскобе, антитела будут обнаружены в крови). Также иммуноферментный анализ дает информацию о длительности и остроте инфекционного процесса.
Лечение хламидиоза проводится по назначению и под контролем врача. Общим обязательным условием является одновременность лечения для обоих супругов или половых партнеров. Прогноз при современном и адекватном лечении благоприятный.
По большому счету профилактика хламидиоза ничем не отличается от профилактики других инфекций, передающихся половым путем. Однако из-за того, что хламидийная инфекция в настоящее время чрезвычайно распространена, а протекает хламидиоз чаще всего бессимптомно, и заметить носителя хламидий “невооруженным взглядом” практически невозможно, профилактике хламидиоза нужно уделить максимальное внимание. Лучший способ профилактики хлoмидиоза, равно как и других ИППП, – это изменение сексуального поведения. Это значит, что необходимо разборчиво относиться к выбору половых партнеров, не допускать случайных связей и пользоваться презервативом, если есть хотя бы малейшая неуверенность в здоровье партнера. “Народные способы” защиты от ИППП, в частности от хламидиоза – такие, как спринцевание, обмывание наружных половых органов водой, использование хлорсодержащих антисептиков, не только очень ненадежны, но могут дать и обратный эффект. Дело в том, что во время спринцевания из влагалища вымывается вся микрофлора, в том числе и та, которая защищает слизистую от вторжения патогенных микроорганизмов. Так что косвенной профилактикой ИППП, в том числа хламидийной инфекции, можно считать поддержание на должном уровне иммунной системы организма, а также правильный уход за половыми органами. Поэтому соблюдение правил гигиены половых органов, регулярные обследования у врача на предмет состояния микрофлоры влагалища, а также здоровый образ жизни, который помогает поддерживать на нужном уровне иммунитет – все это тоже может считаться мерами профилактики множества заболеваний, передающихся половым путем, в том числе и профилактики хламидиоза. Однако даже презерватив не дает 100% гарантию того, что заражение не произойдет. Поэтому людям, имеющим более одного сексуального партнера или не уверенным в его здоровье, необходимо хотя бы несколько раз в год посещать врача и сдавать анализы на ИППП, в том числе и на хламидиоз. Хорошо, если анализ на ИППП будет принято сдавать перед вступлением молодых людей в брак – это поможет укрепить здоровье молодых семей, что очень важно, если в будущем они планируют стать родителями. Если анализ на хламидии для молодых супругов желателен, то при планировании беременности, такой анализ обоим супругам нужно сдать обязательно. Это очень важно для того, чтобы в случае необходимости пролечиться от хламидиоза до наступления беременности. Такой ответственный подход родителей к здоровью будущего человечка – лучшая профилактика хламидийной инфекции у плода и новорожденного.
Простатит и хламидиоз
2 ГБОУ ВПО «Саратовский государственный медицинский университет им. В.И. Разумовского» Министерства здравоохранения России
В данной статье приведены результаты микробиологического и клинического обследования 122 больных хроническим простатитом, ассоциированным с Chlamydia trachomatis, проведенного с целью выявления микробных ассоциаций и их взаимосвязи с симптоматикой заболевания. У всех пациентов определялась выраженность клинической симптоматики по опроснику СОС-ХП; проведено комплексное микробиологическое исследование секрета простаты. В результате исследования выявлена высокая частота встречаемости бессимптомных форм течения хронического простатита у пациентов с хламидийной моноинфекцией. Также отмечено наличие зависимости величины балла по шкале СОС-ХП от наличия ассоциации микроорганизмов, что подтверждает важность комплексного микробиологического обследования пациентов с хроническим простатитом.

1. Кисина В.И. Воспалительные заболевания органов малого таза и связь их с инфекциями, передаваемыми половым путем. Часть I. Этиология, патогенез // Вестник дерматологии и венерологии. – 2002. – № 3. – С. 25–30.
2. Игнатовский А.В. Об особенностях микробных ассоциаций при урогенитальном хламидиозе // Материалы I конгресса дерматовенерологов. – СПб., 2003. – С. 113–114.
3. Peeling R.W., Toye B., Jessamine P. et al. Pooling of urine specimens for PCR testing: a cost saving strategy for Chlamydia trachomatis control programmes // Sex.Transm.Inf. – 1998. – Vol. 74. – P. 66–70.
4. Butler C., Dewsnap C., Evangelou G. Are all genital Chlamidia trachomatis infections pathogenic? A study in men // Sex. Transm. Infect. – 2003. – Vol. 79. – P. 349.
5. Халдин А.А. Современное состояние проблемы негонококковых уретритов и перспективы их терапии // Российский журнал кожных и венерических болезней. – 2004. – № 3. – С. 42–45.
Как известно, в развитии хронического простатита (ХП) могут принимать участие как возбудители ИППП (в первую очередь хламидии и трихомонады), так и ассоциированные с ними условно-патогенные микроорганизмы. В связи с этим существенное значение для обеспечения эффективности лечения хронического простатита имеют комплексная диагностика и комплексная терапия заболевания. В последнее время большое внимание уделяется вопросу влияния смешанной микрофлоры на течение болезней мочеполовой сферы в связи с тем, что в условиях нарушения местного и общего иммунитета значительно возрастает роль ассоциаций микроорганизмов в возникновении и поддержании (хронизации) воспалительного процесса [1, 2]. Кроме того, широкому распространению урогенитального хламидиоза во многом способствует несвоевременная диагностика, имеющая место во многом вследствие поздней обращаемости больных к врачу из-за бессимптомного течения болезни, которое имеет место у 34–70 % пациентов [3, 4, 5].
С учетом этих положений целями нашей работы являлись: определение характера смешанной микрофлоры при ХП, ассоциированным с С. trachomatis, и изучение взаимосвязи проявлений болезни с микст-инфекцией. Для этого проведено комплексное клиническое и микробиологическое обследование больных ХП, обратившихся к врачу с наличием урогенитальной симптоматики, и пациентов с отсутствием субъективных жалоб, обратившихся по различным причинам для обследования или выявленных активно (при обследовании половых партнеров в порядке конфронтации).
Материалы и методы исследования
В исследование включено 122 пациента. Рандомизировано две группы наблюдаемых больных ХП, ассоциированным с хламидиозом. Первая группа представлена 74 мужчинами с наличием урогенитальной симптоматики: клинический индекс хронического простатита (КИ-ХП) по системе СОС-ХП был выше 10 баллов. Во вторую группу включено 48 «случайно отобранных» мужчин с ХП, подтвержденным лабораторно и методом ТРУЗИ, с наличием хламидийной инфекции; отличием пациентов второй группы был низкий КИ-ХП по системе СОС-ХП: меньше 10 баллов.
Результаты исследования и их обсуждение
При микробиологическом исследовании секрета простаты и/или постмассажной порции мочи при постановке «четырехстаканной пробы» у 69 (93,2 %) наблюдаемых первой группы была обнаружена условно-патогенная микрофлора (УПМ) (в количестве 1∙104 м.к./мл и выше). Во второй группе («бессимптомной») условно-патогенные микроорганизмы выявлены только у 9 (16,7 %) мужчин. Различия по показателю детекции УПМ между I и II группами статистически значимы (p < 0,05).
Наиболее часто имела место смешанная инфекция, представленная наряду с С.trachomatis двумя видами микроорганизмов – в 46,2 % случаев; реже одновременно присутствовали три вида – в 29,5 % случаев; один вид – у 23,1 % наблюдаемых и четыре вида – у 1,3 %.
Показана следующая частота выявления отдельных микроорганизмов, ассоциированных с хламидиями: T. vaginalis – 9,0 %, Ureaplasma urealyticum – 10,3 %, Myсoplasma hominis – 11,5 %, Gardnerella vaginalis – 9,0 %, Staphylococcus spp. – 53,8 %, Streptococcus spp. –11,5 %, Candida spp. – 3,8 %, Enterococcus spp. – 32,1 %, E. Сoli –15,3 %, другие Enterobacteriaceae spp. – 23,1 % (рисунок).
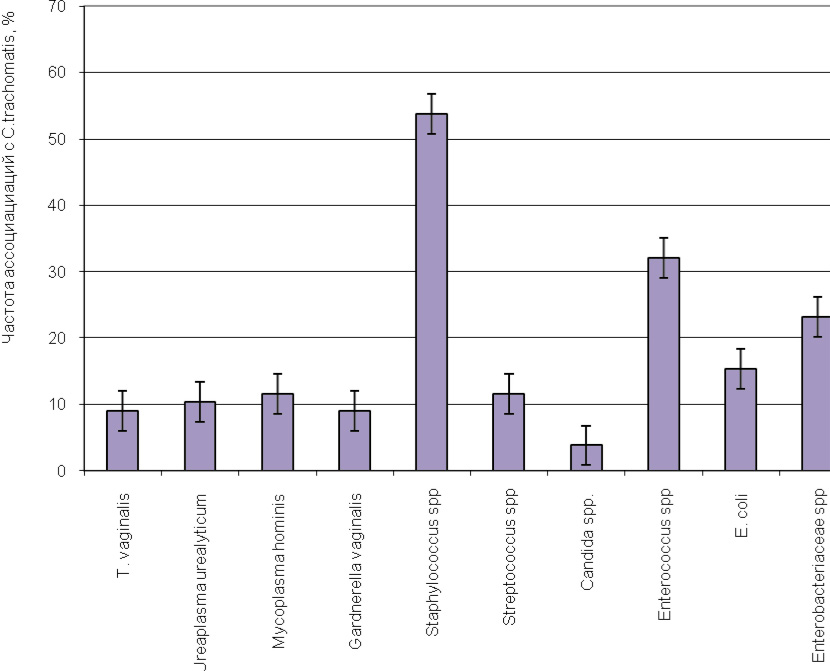
Частота ассоциаций (в %) С. trachomatis с другими микроорганизмами у больных хроническим простатитом
Следует отметить, что основными микроорганизмами, ассоциированными с хламидийной инфекцией при ХП, чаще всего были стафилококки, преимущественно эпидермальный (35,9 %) и гемолитический (12,8 %), а также энтерококки. Анализ антибиотикорезистентности выделенных микроорганизмов показал относительно большой процент штаммов-изолятов, нечувствительных к широко используемым на практике группам антибактериальных препаратов.
Суммируя данные по двум группам наблюдения (n = 122), можно сделать заключение, что при хламидийной моноинфекции (n = 48) умеренная и выраженная симптоматика имела место у 5 (10,4 %) больных, а при смешанной хламидийной инфекции (n = 74) умеренная и выраженная симптоматика отмечалась у 69 (93,2 %) пациентов (p < 0,05).
Известно, что наличие микст-инфекции с участием условно-патогенных бактерий сопровождается более тяжёлым течением простатита у мужчин с хронизацией инфекционного процесса. Полученные результаты свидетельствуют о высокой частоте бессимптомных форм ХП при хламидийной инфекции и о взаимосвязи наличия сопутствующей условно-патогенной микрофлоры с симптоматикой, оцениваемой по СОС-ХП. Кроме того, данные о бессимптомных формах ХП могут являться основанием для предположения о роли мужчин с данной патологией в качестве «резервуара» хламидийной инфекции, а также подтверждают актуальность вопроса расширения показаний для обследования на урогенитальный хламидиоз при ХП с целью профилактики осложнений, сопутствующих этой инфекции.
Следует заметить, что, говоря о ХП, ассоциированном с хламидийной инфекцией, мы не ставили своей задачей представить хламидии в качестве этиологического фактора простатита. Причиной этого была недоступность средств количественного определения С.trachomatis при постановке «четырехстаканной» пробы, принятой за основу при определении инфекционного генеза хронического простатита и роли отдельных микроорганизмов в развитии данной патологии. Внедрение тест-систем на основе Real time-PCR, возможно, откроет путь к решению этой проблемы.
Таким образом, приведённые данные позволяют сделать заключение о высокой частоте выявления условно-патогенных микроорганизмов при урогенитальном хламидиозе. Высокая частота выявления смешанной микрофлоры при урогенитальном хламидиозе, отмеченная нами взаимосвязь наличия условно-патогенных бактерий с выраженностью клинических проявлений болезни указывают на важность комплексных микробиологических исследований, направленных как на обнаружение возбудителей ИППП, так и на идентификацию неспецифичной микрофлоры с определением её чувствительности к антибиотикам.
Рецензенты:
Спирин П.В., д.м.н., доцент кафедры урологии, ГБОУ ВПО «Саратовский ГМУ им. В.И. Разумовского» Минздрава РФ, г. Саратов;
Завьялов А.И., д.м.н., профессор кафедры кожных и венерических болезней, ГБОУ ВПО «Саратовский ГМУ им. В.И. Разумовского» Минздрава РФ, г. Саратов.
Простатит и хламидиоз
Челябинский областной кожно-венерологический диспансер
Челябинская государственная медицинская академия
Челябинская государственная медицинская академия
Современные методы лечения больных хроническим хламидийным простатитом
Журнал: Клиническая дерматология и венерология. 2010;8(5): 32-37
Зиганшин О. Р., Безпалько Ю. В., Ковалев Ю. Н. Современные методы лечения больных хроническим хламидийным простатитом. Клиническая дерматология и венерология. 2010;8(5):32-37.
Ziganshin O R, Bezpal’ko Iu V, Kovalev Iu N. Modern methods for the treatment of patients with chronic chlamydial prostatitis. Klinicheskaya Dermatologiya i Venerologiya. 2010;8(5):32-37. (In Russ.).
Челябинский областной кожно-венерологический диспансер





Челябинский областной кожно-венерологический диспансер
Челябинская государственная медицинская академия
Челябинская государственная медицинская академия
Хронический простатит — самое распространенное урологическое заболевание у мужчин моложе 50 лет и третье по частоте среди урологических диагнозов у мужчин старше 50 лет; составляет 8% амбулаторных визитов к урологу [1]. С увеличением возраста частота заболевания увеличивается и достигает 30—73% [2—4]. По влиянию на качество жизни это заболевание сопоставимо с инфарктом миокарда, стенокардией, болезнью Крона, что обусловливает также значительные психологические и социальные проблемы у больных простатитом мужчин трудоспособного возраста [5]. На долю хронического бактериального простатита приходится 5—15% случаев заболевания [6]. Одной из причин, способствующих увеличению частоты развития воспалительных процессов в органах малого таза и простате, являются урогенитальные передающиеся половым путем инфекции, вызываемые хламидиями, трихомонадами, микоплазмой и др. Это связано как с изменением полового поведения в обществе, так и с появляющейся резистентностью возбудителя к лекарственным препаратам [7, 8]. Кроме того, противомикробные препараты плохо проникают в простату и концентрация их в железе значительно ниже, чем в сыворотке крови [1, 9].
Урогенитальный хламидиоз относится к наиболее распространенным болезням мочеполовой системы мужчин [2]. Течение хронического хламидийного простатита (ХХП), как и простатитов, вызванных другими инфекционными агентами, не бывает монотонным с одинаковой интенсивностью клинических проявлений. Как правило, этому заболеванию свойственны периодические обострения с заметным усилением субъективных и объективных расстройств, сменяющихся периодом затишья. При ХХП развиваются значительные изменения иммунологических показателей, формируется вторичный иммунодефицит, который проявляется дисфункцией системного и местного иммунитета. Рациональное применение иммуностимулирующей терапии в комплексе с антибиотиками и местным медикаментозным лечением по сравнению с моноантибиотикотерапией способствует не только этиотропному излечению ХХП, но и более полной реабилитации больных [3, 7, 10].
Метод иммунокоррекции с использованием иммуномодулятора циклоферона был использован нами как дополнение к комплексной терапии хронического урогенитального хламидиоза. Нами исследована клиническая и иммунологическая эффективность циклоферона при ХХП.
Материал и методы
Исследование проведено у 50 пациентов с хроническим простатитом, у которых методами полимеразной цепной реакции (ПИФ) и прямой иммунофлюоресценции (ПЦР) с праймерами на основе плазмиды C. trachomatis был обнаружен хламидиоз. Материалом для диагностики служили осадок первой порции мочи, секрет простаты, эякулят. Основным критерием инфекционного процесса было выявление в 3-й порции мочи посkt массажf, секрете простаты патогенной микрофлоры (хламидий, трихомонад и др.) или условно-патогенной в концентрации 1·10 4 микробных тел/мл и выше. Средний возраст больных мужчин составил 36,05±0,8 года, средний возраст здоровых — 29,8±0,8 года. Больные ХХП получали комплексную терапию: антибактериальный препарат офлоксин в дозе 400 мг 2 раза в сутки в течение 15 дней, индуктор интерферонов циклоферон, который вводили в виде раствора (125 мг/мл) для внутримышечных инъекций в дозе 2 мл по традиционной схеме, на курс 10 инъекций, кроме того осуществляли коррекцию микроциркуляции и воспаления посредством противовоспалительных препаратов (свечи дикловит, найз), ферментативных препаратов (лонгидаза), α-адреноблокаторов (зоксон по 2 мг ежедневно); одновременно назначали физиотерапию в виде низкоинтенсивного инфракрасного лазерного излучения и магнитотерапию на область промежности (аппарат Интрамаг, Мустанг), массажи простаты, инстилляции в уретру проторгола.
У всех пациентов исследовали состояния местного и системного иммунитета до лечения и через 1 мес после окончания терапии. В периферической крови определяли уровень различных субпопуляций лимфоцитов, активность, интенсивность фагоцитоза, НСТ-тест, иммуноглобулины (Ig) классов А, М, G. В эякуляте больных ХХП определяли общее число лейкоцитов, процент жизнеспособных клеток, лизосомальную активность нейтрофилов, активность фагоцитоза, НСТ-тест.
Контрольную группу составили 50 здоровых мужчин без урогенитальной патологии и урогенитальных инфекций.
Всем пациентам проводили трансабдоминальное ультразвуковое исследование (УЗИ) для определения количество остаточной мочи. Всех пациентов подвергали трансректальному УЗИ простаты.
Эффективность метода лечения подтверждали результатами ПИФ и ПЦР, свидетельствующих об эрадикации хламидий из организма человека. Контроль излеченности проводили через 2 мес после окончания лечения.
Результаты и обсуждение
Эффективность терапии оценивали по этиологическому и клиническому выздоровлению больных (купирование болевого синдрома, дизурии, восстановление половой функции, исчезновению психосоматических расстройств), нормализации клинико-лабораторных показателей. Жалобы сопоставляли до лечения и через 2 мес после окончания терапии.
На основании жалоб, данных анамнеза и результатов лабораторных исследований, хронический катаральный (поверхностный) простатит был диагностирован у 12 (24%) больных, фолликулярная форма — у 28 (56%), паренхиматозный простатит — у 10 (20%).
При исследовании секрета простаты у всех пациентов был выявлен лейкоцитоз, умеренное количество липоидных зерен — у 23 (46%) и небольшое количество — у 27 (54%); кроме того, было характерно наличие слизи, слущенного эпителия, флоры.
Наиболее частыми симптомами у наблюдаемых больных хроническим простатитом были боль (в промежности, над лобком, в паховой области, в области заднего прохода, в пояснице, по внутренней поверхности бедер, в половом члене, в яичках) у 90% больных, дизурические явления — у 31 (62%).
Остаточная моча после акта мочеиспускания отсутствовала или определялась в минимальном количестве (до 10 мл) у 24 (48%), 11—50 мл — у 21 (42%), 51—100 мл у 5 (10%) больных хроническим простатитом. У больных, отмечавших чувство неполного опорожнения мочевого пузыря после акта мочеиспускания, среднее количество остаточной мочи составило 40,1±4,84 мл, а у больных без этого ощущения —11,03±1,41 мл.
Трансректальное УЗИ позволило выявить гиперэхогенные изменения в структуре железы у 88% больных, микрокальцинаты — у 14%. Наиболее характерными находками на эхограммах больных хроническим простатитом были участки чередования мелких зон повышенной эхогенности (участки фиброза, клеточной инфильтрации) и пониженной плотности (зоны воспалительного отека, инфильтрации и ретенционных кист).
У больных, получавших комплексную терапию с использованием циклоферона, через 2 мес после лечения наблюдалось значительное улучшение состояния: исчезали болевые ощущения, императивные позывы на мочеиспускание и позывы на мочеиспускание в предутренние часы, остальные симптомы дизурии значительно ослабели (табл. 1, 2).
После лечения циклофероном только у 2 (4%) пациентов сохранялись боли при эрекции, боль во время эякуляции перестала беспокоить после лечения всех пациентов с данными жалобами. Ослабление эрекции в группе больных, получавших циклоферон, сохранялось у 6 (12%) мужчин.
Комплексная терапия с применением циклоферона приводила к улучшению половой функции, при этом значительно уменьшалось количество жалоб на преждевременную эякуляцию, стертый оргазм, снижение полового влечения.
Через 1 мес после комплексного лечения ХХП с применением циклоферона гипоэхогенные образования в простате сохранялись лишь у 4 (8%) больных. Расширение перипростатических вен наблюдалось у 3 (6%) мужчин, получавших циклоферон.
После лечения у пациентов жалобы на неполное опорожнение мочевого пузыря отсутствовали. При УЗИ остаточная моча не определялась у всех пациентов.
Результаты анализа проведенных исследований указывают на высокую эффективность комплексной терапии ХХП с применением циклоферона.
Анализ результатов ПЦР и ПИФ, выполненный через 2 мес, позволил выявить, что при применении комплексной терапии с циклофероном элиминация возбудителя в группе больных ХХП наблюдалась в 49 (98%) случаях, в то время как эффективность традиционных схем лечения ХХП колеблется от 85 до 90%.
Важно отметить, что состояние больного, получавшего циклоферон, в терапии которого не удалось добиться полной элиминации возбудителя, оценивалось как стабильное, связанное с персистенцией хламидий. Жалобы и клинические проявления у данного больного отсутствовали.
Нами была произведена оценка показателей системного и местного иммунитета у мужчин с ХХП и иммунологической эффективности терапии циклофероном.
У больных с ХХП по сравнению с группой здоровых мужчин в эякуляте отмечалось повышенное содержание лейкоцитов, увеличение процента жизнеспособных лейкоцитов и активности лизосом, а также повышение НСТ-спонтанной и НСТ-индуцированной активности нейтрофилов. Необходимо отметить, что при этом снижались функциональный резерв нейтрофилов, активность и интенсивность фагоцитоза, процентное содержание нейтрофилов в эякуляте больных ХХП.

После лечения у пациентов, получавших терапию циклофероном, наблюдалось уменьшение количества лейкоцитов, нейтрофилов, снижалась активность лизосом нейтрофилов, НСТ-спонтанная и НСТ-индуцированная активность нейтрофилов, а также процент жизнеспособных лейкоцитов. После лечения пациентов, получавших терапию циклофероном, наблюдалось также увеличение процента содержания нейтрофилов, активности и интенсивности фагоцитоза нейтрофилов и функционального резерва нейтрофилов (табл. 3).
В периферической крови у пациентов с ХХП по сравнению с группой здоровых доноров снижалось содержание лейкоцитов, лимфоцитов, увеличивалось содержание моноцитов при неизменном уровне эозинофилов в периферической крови. Отмечались также изменения в показателях субпопуляций лимфоцитов: понижалось содержание лимфоцитов CD3+, CD4+, регистрировалось уменьшение соотношения CD4+/CD8+. Увеличивалось содержание Ig классов А, М, G, а также циркулирующие иммунные комплексы (ЦИК) у больных ХХП. По сравнению с группой здоровых доноров у больных этой группы увеличивалась НСТ-спонтанная и НСТ-индуцированная активность нейтрофилов при снижении их функционального резерва, а также отмечалось снижение активности и интенсивности фагоцитоза в периферической крови.

Оценка системного иммунитета пациентов, получавших циклоферон, показала, что препарат способствовал увеличению количества лейкоцитов в периферической крови, повышению содержания лимфоцитов, увеличению функционального резерва нейтрофилов за счет снижения спонтанной активности нейтрофилов в НСТ-тесте, повышению активности фагоцитоза (табл. 4).

После лечения с использованием циклоферона в периферической крови пациентов отмечалось, по сравнению с группой больных возрастание лимфоцитов CD3+, СD4+, а также существенное возрастание соотношения CD4+/CD8+ (табл. 5).

Колебания уровней иммуноглобулинов и ЦИК после лечения циклофероном отражены в табл. 6. Отмечалось снижение уровней Ig класса А, существенное снижение уровня Ig класса M, ЦИК в периферической крови.
Выводы
Эффективность комплексного лечения больных ХХП с использованием циклоферона доказана не только клиническим выздоровлением, но и высоким процентом элиминации возбудителя из мочеполового тракта, а также улучшением показателей местного и системного иммунитета. Результаты анализа данных показывают, что циклоферон воздействует на большинство звеньев иммунитета. Представленные материалы подтверждают высокую эффективность циклоферона и необходимость применения этого иммунотропного препарата при лечении больных ХХП.
Лечение хронического простатита на фоне хламидийной инфекции

Весь контент iLive проверяется медицинскими экспертами, чтобы обеспечить максимально возможную точность и соответствие фактам.
У нас есть строгие правила по выбору источников информации и мы ссылаемся только на авторитетные сайты, академические исследовательские институты и, по возможности, доказанные медицинские исследования. Обратите внимание, что цифры в скобках ([1], [2] и т. д.) являются интерактивными ссылками на такие исследования.
Если вы считаете, что какой-либо из наших материалов является неточным, устаревшим или иным образом сомнительным, выберите его и нажмите Ctrl + Enter.
Лечение хронического простатита, как и многих заболеваний, зачастую оказываются неэффективным, поскольку не учитывает индивидуальных особенностей организма и направлены в основном этиотропно, при этом незаслуженно пренебрегают патогенетической терапией.
Урогенитальный хламидиоз – проблема, не теряющая актуальности. В немалой степени этому способствует внутриклеточная локализация и персистенция возбудителя, из-за чего монотерапия самыми современными антибиотиками оказывается недостаточно эффективной. К персистенции хламидий приводит лечение препаратами, малоактивными в отношении этого инфекционного агента, субтерапевтические дозы антихламидийных препаратов, отсутствие иммунотерапии.
В природе существует две формы клеточной гибели – апоптоз и некроз. Апоптоз – закономерное умирание клетки в положенные сроки путем сморщивания и фрагментирования. Погибшие в результате апоптоза клетки не причиняют вреда окружающим тканям, их обломки поглощаются макрофагами. Внутри макрофагов микроорганизмы, будь то микобактерии или хламидий, погибают. Напротив, некроз клеток приводит к выбросу в окружающую среду химически агрессивных компонентов цитоплазмы и диссеминации, находящихся в клетке микроорганизмов, что ведет к распространению инфекции. Отсюда ясно, насколько велика роль апоптоза и ценность препаратов, регулирующих этот процесс.
Недавно появившаяся на лекарственном рынке биологически активная добавка индигал, содержащая в каждой капсуле не менее 90 мг чистого индол-3-карбинола и не менее 15 мг чистого эпигаллокатехина-3-галлата, способствует нормализации процессов апоптоза, что было показано в ряде зарубежных исследований. В эксперименте in vitro и in vivo продемонстрировано выраженное ингибиторное действие индол-3-карбинола на раковые клетки простаты и стимулирующий эффект на процессы апоптоза. Эпигаллокатехин-3-галлат, вторая составляющая индигала, уменьшает клеточную пролиферацию, индуцирует апоптоз, купирует воспалительные каскады.
В отношении хламидий наиболее активны макролиды, затем идут фторхинолоны, также действующие бактерицидно. Среди фторхинолонов особое место в отношении внутриклеточных возбудителей занимает спарфлоксацин, степень проникновения которого в макрофаг в 3 раза превышает таковую у ципрофлоксацина и ломефлоксацина. Кроме того, за счет двойной блокировки ДНК микроорганизма спарфлоксацин предотвращает развитие лекарственной резистентности.
Помимо антибактериального эффекта и предотвращения некроза, необходимо еще одно патогенетическое воздействие, направленное на ускоренную элиминацию продуктов распада, купирование воспаления и восстановление локальной иммунорезистентности. Этими свойствами в полной мере располагает растительный препарат канефрон-Н, содержащий водно-спиртовой экстракт травы золототысячника, корней любистока лекарственного и листьев розмарина.
Медикаментозное лечение хронического простатита на фоне хламидийной инфекции
Целью исследования было разработать и апробировать схему лечения больных урогенитальным хламидиозом, резистентным к стандартной терапии. Под наблюдением находилось 14 мужчин с верифицированным урогенитальным хламидиозом. У 5 из них преобладали клинические признаки уретрита, а у 9 – уретропростатита. Диагноз был установлен в сроки от 3 до 11 лет, в среднем за 7,4±1,2года. Пациенты получали неоднократные курсы антибактериальной терапии, в результате чего у 6 из них развился дисбактериоз кишечника II-III степени, у 2 – кандидоз, у 4 – непереносимость антибактериальных препаратов группы макролидов по токсико-аллергическому типу. Если у 6 мужчин не исключалась реинфекция, то 8 из них не имели незащищенных и/или случайных половых контактов и, следовательно, их заболевание расценивалось как хроническое и резистентное к терапии. Только у 2 больных была хламидийная моноинфекция. У остальных 12 пациентов в отделяемом мочеиспускательного канала и/или эксприматах половых желез исследование выявило следующих возбудителей заболевания:
- стафилококки – 4 случая;
- энтерококки – 2 случая;
- Mycoplasma hominis – 4 случая;
- Ureaplasma – 4 случая;
- стрептококковая инфекция – 1 случай;
- Е. coli – 1 случай.
У большинства мужчин присутствовало одновременно более двух инфекционных агентов.
Для исключения туберкулеза мочеполовой системы больным до пальцевого ректального исследования выполнялась 3-стаканная проба мочи. При наличии лейкоцитурии во второй порции, что было выявлено у 1 больного, проводились УЗИ почек, посев мочи на микобактерии туберкулеза и люминесцентная микроскопия мазков.
Тщательно собирался эпидемический анамнез, и было установлено, что ни один пациент ранее туберкулезом не болел, контактов с больными туберкулезом людьми и животными не имел, в семье детей с виражом пробы Манту не было. Все 14 пациентов регулярно проходили флюорографию, последнее исследование выполнялось меньше чем за 12 месяцев до обращения.
Учитывая неэффективность предшествующей терапии, решено было в качестве антибиотика избрать спарфлоксацин по 200 мг дважды в сутки в течение 10 сут при уретрите и 20 сут при уретропростатите. Выбор пал на спарфлоксацин, поскольку он:
- бактерициден по отношению к хламидиям;
- воздействует не только на активно делящиеся, но и на персистирующие микроорганизмы;
- обладает высокой способностью проникать внутрь клетки.
С целью нормализации апоптоза назначался индигал по 800 мг дважды в сут в течение 2 мес, поскольку именно этот период необходим для отмирания инфицированной хламидиями клетки. Для улучшения отторжения слущенного эпителия, восстановления микроциркуляции и купирования воспаления больные принимали канефрон-А по 50 капель 4 раза в сут в течение 1 мес.
Окончательные результаты оценивались через 2 мес после начала комплексной терапии. Учитывались динамика жалоб, анализ секрета простаты при нативной световой микроскопии и окрашенного по Граму мазка (количество лейкоцитов, насыщенность лецитиновыми зернами, присутствие и вид микрофлоры), спермограмма, бактериологические исследования, анализ отделяемого мочеиспускательного канала, УЗИ простаты, исследование соскоба мочеиспускательного канала и секрета простаты методом ПЦР, иммуноферментный анализ (ИФА) крови.
При поступлении все 14 мужчин жаловались на выделения из мочеиспускательного канала – от скудных до обильных, учащенное мочеиспускание (у 8 пациентов – с резью), в том числе ночью, постоянную ноющую боль в промежности (у 6 больных- с иррадиацией в мошонку), нарушение сексуальной функции.
При первичном пальцевом ректальном исследовании у всех больных определялись нарушение тонуса простаты, ее болезненность, у 12 пациентов пальпировались плотные очаги. Губки мочеиспускательного канала у всех были отечны и гиперемированы. В секрете простаты обнаруживали большое количество лейкоцитов (от 43,7+9,2 до уровня, когда подсчет невозможен), число лецитиновых зерен было снижено.
Всем пациентам был назначен комплекс этиопатогенетической терапии, описанный выше; всем рекомендовалось избегать нахождения на солнце (учитывая потенциальный фототоксический эффект спарфлоксацина), половой покой (или, в крайнем случае, использование презерватива), обильное питье. Все половые партнеры пациентов также проходили обследование и лечение в необходимом объеме.
Клиническая эффективность проявлялась с 5,4±0,2 сут, и выражалась в уменьшении дизурии, боли и прекращении уретральных выделений. К завершению антибактериального этапа терапии у ^больных (85,7%) отмечалась полная санация секрета простаты, а у оставшихся 2 (14,3%) – существенное улучшение. Через 2 мес только у 1 пациента (7,1%) сохранялось умеренно повышенное число лейкоцитов в секрете простаты. ТРУЗИ, выполненное в эти же сроки, показало выраженную положительную динамику в отношении эхоструктуры и кровоснабжения предстательной железы. У всех больных наступило микробиологическое очищение – ни в окрашенных мазках, ни методом посева, ни методом ДНК-диагностики не была обнаружена какая-либо патогенная микрофлора. Также не отмечено отрицательного влияния апробируемой схемы на сперматогенез – качественные и количественные показатели эякулята не имели достоверных различий по сравнению с исходными.
Переносимость лечения была хорошей. У пациента отмечались явления диспепсии при приеме препаратов натощак; прием после еды позволил избежать этой побочной реакции без снижения дозы или назначения дополнительной терапии.
Таким образом, сочетание спарфлоксацина с индигалом способствует предотвращению персистенции внутриклеточных микроорганизмов и их диссеминации, что приводит к быстрому снижению общей популяции Chl. trachomatis. Канефрон-Н обеспечивает купирование воспаления, диуретический эффект, ускоренную элиминацию продуктов распада и слущенного эпителия. Указанная комбинация в совокупности обеспечила клинико-бактериологическое излечение больных урогенитальным хламидиозом, резистентным к стандартной терапии, в 92,9% случаев.

[1], [2], [3], [4], [5], [6], [7], [8], [9], [10], [11], [12], [13], [14], [15], [16]
Озонотерапия
Проанализирована эффективность озонотерапии и предложено патогенетическое обоснование ее как фактора, улучшающего гемодинамику и микроциркуляцию. В исследование были включены 72 больных хроническим уретропростатитом на фоне хламидийной инфекции, получавшие идентичную базовую терапию: кларитромицин (фромилид-А), меглюмина акридонацетат (циклоферон), вобэнзим.
- Первую группу составили 34 пациента, имеющие хронический уретропростатит (клинические симптомы уретрита и простатита были выражены одинаково) на фоне хронического простатита хламидийной природы. Они получали комплексную базовую терапию по лечению инфекций, передающихся половым путем: кларитромицин (фромилидж), меглюмина акридонацетат (циклоферон), вобэнзим.
- Вторая группа включала 20 пациентов с хроническим уретропростатитом на фоне хронического простатита хламидийной природы. У них преобладали жалобы в отношении мочевыводящих путей, клинические проявления простатита были менее выражены. У этих больных базовая терапия была дополнена региональной трансуретральной озонотерапией.
- Третья группа насчитывала 18 пациентов с хроническим уретро-простатитом на фоне хронического простатита хламидийной природы с доминирующими жалобами, указывающими на поражение простаты. В этой группе базисное лечение было дополнено региональной трансректальной озонотерапией.
- Группа сравнения состояла из 11 мужчин в возрасте от 21 до 45лет без патологии со стороны мочеполовой системы (подтверждено ТРУЗИ предстательной железы и ЛДФ мочеиспускательного канала и простаты) и с отрицательными результатами ИФА и ПЦР к ДНК Chl. trachomatis.
Всем 72 пациентам с хроническим простатитом на фоне хламидиоза и в группе сравнения проводили исследование микрогемодинамики мочеиспускательного канала и простаты методом ЛДФ и ТРУЗИ ПЖ до лечения и повторно в сроки 5-6 нед по окончании терапии.
Этиологическую эффективность лечения оценивали через 6 нед после окончания курса терапии по анализу соскобного материала из мочеиспускательного канала и секрета предстательной железы методом ИФА и ПЦР по следующим показателям:
- эрадикация – отсутствие Ch. trachomatis в контрольных исследованиях;
- отсутствие эффекта – сохранение возбудителя в контрольных исследованиях.
Клиническую эффективность лечения хронического простатита хламидийной природы оценивали по динамике основных жалоб (боль, дизурия, сексуальная дисфункция).
Для более полного сбора анамнеза была использована анкета-опросник по системе суммарной оценки симптомов при хроническом простатите (СОС – ХП), предложенная О.Б.Лораном и А.С. Сегалом (2001), которая включает ряд вопросов по наличию, выраженности и постоянству симптомов, а также по качеству жизни пациентов. Вопросы обозначены цифрами от I до XII и подразделены на четыре группы: боль и парестезия, дизурия, патологические выделения из мочеиспускательного канала (простаторея) и качество жизни. Пациент самостоятельно письменно отвечал на каждый вопрос. Вопросы I и II предусматривали возможность нескольких вариантов ответа, которые обозначены буквами общепринятого английского алфавита. Каждый из положительных ответов оценивался в 1 балл. На вопросы с III по XII дается только один вариант ответа, оцениваемый от 0 до 3-5 баллов, то есть от полного отсутствия до крайней степени выраженности анализируемого показателя.
Заполненную пациентом анкету анализировали. В первую очередь подсчитывали сумму набранных баллов по основным группам вопросов: боль и парестезия, дизурия, качество жизни. Затем определяли индекс симптоматики (ИС – ХП) – сумму баллов, отражающих боль, дизурию и простаторею. Последним устанавливали клинический индекс хронического простатита (КИ – ХП) – сумма ИС – ХП и индекса качества жизни. В зависимости от степени выраженности клинических проявлений КИ – ХП разделен на незначительный, умеренный и значительный. Таким образом, все клинические проявления ХП представлены следующим цифровым рядом:
- боль = ;
- дизурия = ;
- простаторея = ;
- качество жизни =
- ИС-ХП = ;
- КИ-ХП = .
Данная система использована у 60 больных на хронический простатит хламидийной природы. Анкета была понятна пациентам, вопросы и ответы исключали двусмысленность их толкования, а полученные результаты были четкими.
При сборе анамнеза также большое внимание уделяли перенесенным ранее заболеваниям урогенитального тракта, состоянию здоровья полового партнера.
При осмотре пациентов учитывали их конституциональные особенности, состояние кожных покровов и видимые слизистые оболочки, выраженность вторичных половых признаков (распределение волосяного покрова, подкожно-жировой клетчатки, тургор кожи, складчатость и пигментация мошонки). Осуществлялось пальпаторное исследование яичек, ректальное пальцевое исследование простаты. Также пальпаторно исследовали половой член с целью исключения его деформации, патологических изменений белочной оболочки. Физикально оценивалось состояние окружающих периферических вен и артерий, в особенности нижних конечностей и мошонки.
У пациентов, отобранных для исследования, наличие Chl. trachomatis подтверждалось комплексным применением лабораторных методов диагностики ИФА и ПЦР.
Диагностика нарушений кровообращения и микроциркуляции проводилась посредством ТРУЗИ предстательной железы с ЦДК по стандартной методике и ЛДФ микроциркуляции мочеиспускательного канала и предстательной железы; методики подробно описаны в соответствующем разделе монографии.
Метод проведения регионарной озонотерапии
Для проведения региональной озонотерапии использовался медицинский озонатор серии «Medozons ВМ».


